Qual é o processo de desenvolvimento da nefrite lúpica à fibrose renal?
Mar 19, 2022
Contato: Audrey Hu Whatsapp/hp: 0086 13880143964 E-mail:audrey.hu@wecistanche.com
Xuewei Ding1,2, Yi Ren1,2,3e Xiaojie He1,2*
Doença de Lupus(NL) é uma complicação comum do lúpus eritematoso sistêmico (LES) e um importante fator de risco para morbidade e mortalidade. O abundante nucléico livre de células (DNA/RNA) em pacientes com LES, especialmente o dsDNA, é uma substância chave na patogênese do LES e da NL. A deposição de complexos imunes de DNA/RNA (DNA/RNA-ICs) no glomérulo causa uma série de reações inflamatórias que levam ao distúrbio das células renais residentes e, eventualmente, à disfunção renal.fibrose. O DNA/RNA livre de células é o indutor mais eficaz de interferons do tipo I (IFN-I). Células renais residentes (em vez de células imunes infiltrantes) são a principal fonte de IFN-I norim. O IFN-I, por sua vez, danifica as células renais residentes. Não apenas as células renais residentes são vítimas, mas também participantes dessa guerra de imunidade. No entanto, o mecanismo para a geração de IFN-I emrenalcélulas e o mecanismo patológico de IFN-I promovendofibrosenão foram totalmente elucidados. Este artigo revisa a epidemiologia mais recente da NL e seu processo de desenvolvimento discute o mecanismo de geração de IFN-I em células renais residentes e o papel do IFN-I na patogênese da NL e pode abrir uma nova perspectiva para o tratamento da NL.
Palavras-chave: fibrose, IFN-I, nefrite lúpica, sensores de ácido nucleico, patogênese,renalcélulas residentes

Cistanche tubulosa previne doenças renais, clique aqui para obter a amostra
INTRODUÇÃO
O lúpus eritematoso sistêmico (LES) é uma doença autoimune na qual complexos imunes (CIs) se formam e se depositam em vários órgãos. orimé um dos principais órgãos-alvo.Doença de Lupus(LN) está presente em pelo menos 30% a 60% dos pacientes com LES, e quase todos os pacientes têm envolvimento renal patológico. A incidência de LES e NL varia amplamente entre as regiões do mundo e entre os grupos étnicos (1). Embora o LES seja mais prevalente em mulheres do que em homens em todas as faixas etárias e populações, vários estudos mostraram que homens com lúpus têm mais NL do que mulheres com lúpus, e os pacientes com NL são mais jovens, principalmente de raça/etnia africana, asiática e hispânica (2-5). A NL tem uma taxa de mortalidade seis vezes maior que a da população geral (6). A NL é um importante fator de risco para a mortalidade por LES, com 10 por cento dos pacientes com NL desenvolvendo a doença renal terminal (ESRD) (1, 7). Em comparação com pacientes com LES sem NL, os pacientes com NL tiveram uma taxa de mortalidade padrão mais alta ({10}},8 versus 2,4) em um momento de morte anterior (6, 8–10). Nos últimos anos, o diagnóstico precoce, o tratamento padronizado e novos imunossupressores como micofenolato mofetil, anticorpo monoclonal anti-CD20, belimumabe e outras drogas melhoraram significativamente o prognóstico da NL. No entanto, a taxa de mortalidade de 5- anos em pacientes com NL refratária grave permanece alta (1, 3, 11, 12). Portanto, elucidar sua patogênese pode fornecer uma base teórica para a triagem de alvos terapêuticos eficazes para NL.
O IFN-I é um fator central na ocorrência e desenvolvimento do LES. Estudos recentes sugerem que o IFN-I pode desempenhar um papel ao nível dos órgãos terminais no LES, especialmente no NL. O IFN-I é uma resposta à ativação da maioria das células imunes. Atualmente, os estudos sobre a relação entre IFN-I e LN concentram-se principalmente em células imunes no soro erins. As células renais residentes também têm funções imunológicas e estão envolvidas na guerra imunológica. A literatura anterior mostrou que as células renais residentes (em vez de células imunes infiltrantes) são a principal fonte de IFN-I norime que o IFN-I pode causar lesão renal. No entanto, existem poucos estudos sobre a produção de IFN-I no rim e o dano do IFN-I às células renais residentes. Este artigo revisa a relação entre IFN-I e células renais residentes de LN e explora as vias relacionadas de IFN-I promovendo a patogênese de LN.
PATOGÊNESE DA LN
Deposição IC
A exposição ao ácido nucleico, a produção de anticorpos patogênicos nefrogênicos e a formação de CIs são as principais ligações que levam à NL. Três mecanismos foram propostos para a formação ou deposição de CIs no glomérulo, e incluem (1) a deposição de imunocomplexos circulantes pré-formados (CICs) no rim, (2) a formação de CIs in situ no glomérulo e ( 3) ligação de anticorpos anti-dsDNA a antígenos de reação cruzada presentes na superfície das células renais residentes ou no ambiente extracelular (13-17).
Autoantígenos e anticorpos circulantes formam CICs, que são depositados no rim. Devido à eliminação inadequada de células necróticas, apoptóticas e/ou aumento anormal da morte celular em pacientes com LES, nucleossomos não degradados (complexos de DNA e pares de peptídeos histonas contendo histonas) são liberados na corrente sanguínea, aumentando os autoantígenos circulantes e anticorpos subsequentes, que formar CICs. Eles evitam o reconhecimento pelo sistema imunológico e são depositados no rim.
CIs também podem ser formados in situ. Estruturas eletrodensas (EDS) associadas à membrana basal glomerular (GBM) e à matriz mesangial constituem o principal alvo para anticorpos Southbound tanto em murinos quanto em humanos.doença de Lupus. Nucleossomos e fragmentos de cromatina se acumulam devido à perda da atividade da desoxirribonuclease 1 (Dnase-1) intra e extrarrenal. Em seguida, nucleossomos e fragmentos de cromatina estimulam prontamente TLR9 em macrófagos infiltrados e células dendríticas, desencadeando a secreção de MMPs locais (18, 19). As MMPs degradam a barreira da membrana, permitindo que nucleossomos e fragmentos de cromatina se liguem ao GBM (20, 21). A exposição à cromatina glomerular in situ induz anticorpos anti-cromatina (anti-dsDNA e anti nucleossomo) a se tornarem nefrogênicos e patogênicos, secundários à formação de CIs in situ (15).
Além de se ligarem a fragmentos de DNA, eles também se ligam a antígenos de reação cruzada na superfície das células renais para ativar a proliferação celular, apoptose, inflamação efibrosecaminhos (13, 14, 17). Os anticorpos anti-dsDNA ligam-se às células mesangiais renais (RMCs) por meio de reação cruzada com a anexina II da superfície celular (22), a-actinina (23, 24) e a proteína P ribossomal (25). Os anticorpos anti-dsDNA ligam-se às células endoteliais glomerulares (GECs) por meio de reação cruzada com proteínas de membrana com PM de 30-35, 44, 68, 110 e 180 kDa (26). Os anticorpos anti-dsDNA ligam-se às células epiteliais tubulares renais (TECs) por meio de reação cruzada com os polipeptídeos SnRNP A e D (27). A polirreatividade dos anticorpos anti-dsDNA pode estar relacionada à similaridade estrutural/conformacional da simulação molecular (28). Ao se ligarem à superfície celular, os anticorpos anti-dsDNA migram para o citoplasma e/ou núcleo, promovendo o crescimento e proliferação celular ou, por sua vez, induzindo a apoptose (29). Estudos recentes relataram que o extrato RG2 da bactéria simbiótica intestinal R. gnavus reage de forma cruzada com anticorpos anti-dsDNA para desencadear ou exacerbar a patogênese imunológica de LN (30, 31).
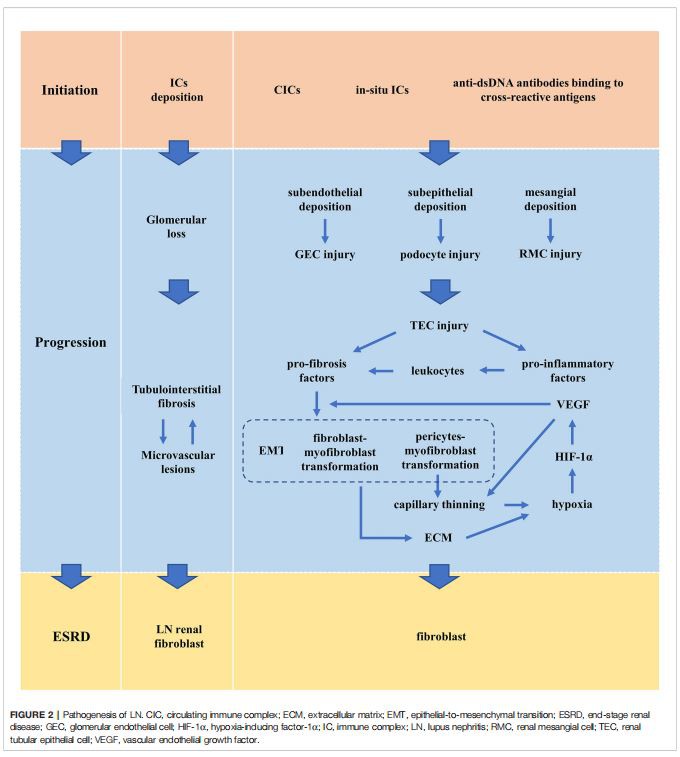
Dependendo do tipo, duração e gravidade da NL, os CIs podem ser encontrados nas regiões subendotelial, subepitelial, mesangial e tubulointersticial (Figura 1). A distribuição, quantidade e propriedades pró-inflamatórias dos CIs no parênquima renal determinam a ativação do complemento, inflamação, proliferação celular e a gravidade das lesões glomerulares e tubulointersticiais (3, 5, 32, 33).

Perda de glomérulo
Os CIs são depositados principalmente no glomérulo. O principal mediador da lesão glomerular induzida por CI é o sistema complemento, especialmente a formação do complexo de ataque à membrana C5b-9. C5b-9 é inserido na membrana glomerular em quantidades extremamente baixas, transformando células normais em células efetoras inflamatórias (34). As células glomerulares imunoestimuladoras produzem grandes quantidades de citocinas pró-inflamatórias (35, 36), acelerando o dano/envelhecimento celular, que pode ser um dos mecanismos de lesão glomerular no NL (37).
A lesão glomerular inicial mediada por CI varia com a localização da deposição de CI. A deposição subendotelial de CI leva ao acúmulo de células pró-inflamatórias, causando doença proliferativa e crescente glomerular (38). O GEC e a camada superficial do GEC (também conhecido como glicocálice) são os primeiros pontos de contato com os componentes do sistema imunológico circulante. As células T são recrutadas para o glomérulo através da ligação direta de seu CD44 ao componente ácido hialurônico (HA) do glicocálice GEC (39). ICs alteram a morfologia celular, regulam positivamente a expressão de caspase ativa-3', inibem a angiogênese e aumentam a produção de NO em GECs (40). A autofagia é um metabolismo conservado que desempenha um papel protetor em muitos tipos de células e doenças. ICs inibem a atividade de autofagia de GECs através da via dependente de Akt/mTOR (41). Os anticorpos LN promovem o aumento da secreção de endotelina{10}} por GECs, levando à ruptura de junções intercelulares apertadas (42). A deposição subepitelial de CI leva a danos nos podócitos e graus variados de proteinúria. A lesão de podócitos é caracterizada por apagamento do processo do pé (FPE), perda de marcadores específicos de podócitos e descolamento de células (43). Os podócitos também contribuem para a formação do crescente glomerular. Os podócitos desdiferenciados migram para crescentes celulares. A lesão de podócitos, em última análise, leva à ativação e proliferação de células epiteliais parietais (PECs) através da via JAK/STAT, a produção de HB EGF e IL-6 e/ou ausência de ligante (CXC) (CXCL) 12 , contribuindo conjuntamente para a formação do crescente glomerular (43). LN IgG estimula o rearranjo do citoesqueleto celular e diminui os níveis de fator de crescimento endotelial vascular (VEGF) em podócitos (42). A deposição mesangial de IC leva à proliferação de RMC e aumento da matriz mesangial. O ambiente inflamatório de LN induz RMCs a produzir citocinas pró-inflamatórias, que recrutam leucócitos (44); promove RMCs para expressar níveis mais elevados de proteínas da matriz e regular enzimas de degradação da matriz, que levam à deposição de matriz mesangial (44, 45); regulam o ciclo celular e promovem a proliferação de RMC (46).
Podócitos, GECs e RMCs no glomérulo interagem e se apoiam. Os podócitos produzem o VEGF necessário para a sobrevivência dos GECs (47, 48); GECs produzem fator de crescimento derivado de plaquetas (PDGF) necessário para a sobrevivência de RMCs; RMCs isolam o fator de crescimento transformante potencial-b (TGF-b), protegendo assim os GECs da apoptose (49). A lesão progressiva de um tipo de célula pode eventualmente levar a danos nos outros tipos de células. A ativação, desdiferenciação ou proliferação de células glomerulares leva à perda da integridade estrutural do aglomerado glomerular e, finalmente, à morte glomerular.
Fibrose Tubulointersticial
O suprimento sanguíneo do tubulointerstício renal é fornecido pelo escoamento glomerular. A perda glomerular afeta a sobrevivência tubulointersticial. Alterações decorrentes da perda da viabilidade intersticial tubular, como atrofia tubular,fibrosee infiltração intersticial. A lesão de células epiteliais tubulares renais (TECs) é uma causa importante defibrose(50, 51). A gravidade e a frequência da lesão dos TECs determinam se esse mecanismo de reparo leva à recuperação ou progressão para fibrose (52). Os TECs executam o mecanismo de reparo para restaurar a função normal quando a lesão é menor ou por um curto período de tempo. Os TECs sofrem reparo mal-adaptativo quando lesões graves e persistentes excedem o mecanismo de reparo normal. O reparo mal adaptativo se manifesta em dois aspectos: parada do ciclo celular na fase G2/M, caracterizada pela expressão de p53, p21 e p16INK4a; fenótipos secretores associados ao envelhecimento, que é caracterizado pela secreção de fatores pró-inflamatórios e fatores pró-fibrose, incluindo TGF-b1, fator de crescimento do tecido conjuntivo (CTGF), CXCL1, IL-6, IL{{15} } (50, 53-56). Esses fatores promovem um microambiente inflamatório crônico propício ao tecido fibroso (53). Os TECs secretam citocinas pró-inflamatórias para recrutar e ativar diferentes células inflamatórias. E essas células recrutadas produzem ainda citocinas que conduzem a transformação de TECs, fibroblastos e pericitos no tipo miofibroblasto (50, 57, 58). Eventualmente, TECs, fibroblastos e pericitos expressam a actina do músculo liso (a-SMA) e promovem a deposição de matriz extracelular (MEC), contribuindo para o processo final de fibrose renal.
Embora os CIs sejam predominantemente detectados no glomérulo, afetando a capacidade glomerular e tubulointersticial, cerca de 70% dos pacientes com NL também apresentam agregados de CIs ao longo da membrana basal tubular, resultando em inflamação tubulointersticial efibrose. Um estudo de biópsia de LN descobriu que CIs tubulares são independentes de CIs circulatórios e glomerulares (59). Anticorpos anti-dsDNA se ligam a A e D SnRNP em TECs, fazendo com que sejam internalizados e transportados para os compartimentos subcelulares citoplasmáticos e nucleares, ou podem permanecer na superfície celular onde a interação com o complemento resulta em lise celular (27) . A ligação de anticorpos anti-dsDNA a TECs induz alterações fenotípicas em TECs que podem promover a transição epitelial-mesenquimal (EMT) (60). Outro estudo mostrou que os anticorpos anti-dsDNA induzem a secreção de TECs de fibronectina solúvel e aumentam a síntese de TGF-b1 e colágeno a jusante por ativação prévia de ERK, p38 MAPK, JNK, PKC-a e PKC-bII (61).
Pericitos são fontes potenciais de miofibroblastos (50, 57, 58). A perda de pericitos leva ao afinamento dos capilares. O afinamento capilar induziu anóxia em TECs, o que aumenta o estresse oxidativo intersticial. Os TECs lesados ou hipóxicos secretam o fator indutor de hipóxia-1a (HIF- 1a) e VEGF subsequente para promover a sobrevivência e proliferação das células endoteliais (ECs), aumentando a densidade capilar perivascular (62, 63). No entanto, a produção excessiva de VEGF promove a formação de vasos permeáveis e não funcionais, resultando em um ambiente hipóxico e altamente oxidativo (64). Além disso, o VEGF pode ser usado como fator pró-inflamatório para agravar afibroseresposta (64). A hipóxia demonstrou promover a EMT como um importante fator microambiental (65-68). O aumento da força da matriz também agrava a hipóxia tubular e a progressão da EMT. Os fatores acima formam um círculo vicioso.
Lesões Microvasculares Renais
Lesões microvasculares renais são comuns na NL e estão sendo cada vez mais reconhecidas como um marcador de NL. Cinco tipos patológicos de lesões microvasculares renais do NL foram propostos e são: depósitos de imunocomplexos vasculares (CDI), arteriosclerose (AS), microangiopatia trombótica (TMA), vasculopatia necrosante não inflamatória (NNV) e vasculite renal verdadeira (TRV). 69). Até um terço dos pacientes com NL apresentam duas ou mais lesões vasculares ao mesmo tempo. Embora cada tipo de lesão possa apresentar seus fatores únicos, existem alguns mecanismos comuns entre as diferentes lesões vasculares. TECs danificados induzem a perda de pericitos levando ao afinamento dos capilares (50, 57, 58, 62-64). A ativação e disfunção de ECs vasculares, bem como a disfunção do sistema imunológico, são mecanismos-chave de lesões microvasculares renais de NL, especialmente inflamação vascular induzida por CI e eventos trombóticos relacionados a anticorpos antifosfolipídios (APL) (69). A ligação de autoanticorpos aos ECs vasculares e a deposição de CICs nos microvasos levam a alterações nas conexões entre os ECs, ativando o complemento, aumentando a expressão de moléculas de adesão, citocinas inflamatórias e quimiocinas e aumentando a permeabilidade dos ECs. A ativação e disfunção das ECs recrutam ainda mais monócitos por meio de moléculas de adesão e quimiocinas, que induzem a agregação plaquetária, resultando em atividade pró-coagulante e microtrombose (70, 71). Os eventos trombóticos induzidos por APL são o mecanismo importante da LN TMA renal (72). Pacientes com MAT tiveram os piores resultados renais (73). As lesões microvasculares renais afetam adversamente os resultados renais a longo prazo e podem determinar a seleção de estratégias de tratamento (73, 74) (Figura 2).
OS MECANISMOS DE GERAÇÃO DE IFN-I NO RIM
Estudos clínicos descobriram que pacientes com NL superexpressam IFN-I, e a atividade de IFN-I está intimamente relacionada à inflamação de LN (75-77). Estudos experimentais em animais mostraram que a exposição ao IFN-I em camundongos NZB/W ou camundongos C57BL/6J acelera glomerulonefrite, crescente glomerular e nefrite intersticial tubular renal (78-80); a redução da atividade biológica do IFN-I em camundongos NZB/W aliviou a patologia renal e melhorou a taxa de sobrevivência (81). Embora um estudo tenha mostrado que o LN mediado pelo receptor Toll-like 7 (TLR7) é independente da sinalização do IFN-I, não é suficiente para mascarar o papel final do IFN-I na aceleração da nefrite (82). IFN-I inclui IFN-a e IFN-b, que desempenham um papel biológico ligando-se aos receptores de interferon tipo I (IFNAR).
Os Mecanismos de Geração de IFN-I
O ácido nucleico livre de células (DNA/RNA) é o indutor mais eficaz de IFN-I. Eles são reconhecidos por sensores de ácido nucleico intracelular, que ativam a via de sinalização que produz IFN-I (Figura 3). Os sensores de DNA incluem o endossomo TLR9, ativador dependente de DNA de fatores reguladores de IFN (DAI), proteína induzível por interferon 16 (IFI16) e GMP-AMP cíclico (cGAMP) sintase (cGAS). Os sensores de RNA incluem TLR3, TLR7, TLR8, um gene I induzível por ácido retinóico (RIG-I) e proteína 5 associada à diferenciação de melanoma (MDA5). A ligação de TLR7/8 com ssRNA e a ligação de TLR9 com DNA CpG ativam vias de sinalização a jusante - proteína adaptadora MyD88 e fatores de transcrição como IRAKs, TRAF6 e IRF7, levando à secreção de IFN-a (83, 84). Ligação de TLR3 com dsRNA induz IFN-b principalmente através da via de sinalização TRIF-TBK1-IRF3. cGAS (85, 86), DAI (87), IFI16 (88) reconhecem o dsDNA e, em seguida, ativam o estimulador de genes de interferon (STING)- TANK-binding kinase 1 (TBK1)-IRF3 para regular a transcrição de Genes induzidos por IFN-b e IFN. RIG-I e MDA5 reconhecem dsRNA e sofrem alterações conformacionais para induzir sinalização antiviral mitocondrial (MAVS), então ativam IRF3/7 por TRAF6/3, resultando na produção de IFN-I (89).
Os pacientes com LES são ricos em cromatina ou ácidos nucleicos livres de células, especialmente dsDNA, devido à depuração defeituosa de células apoptóticas e células necróticas e aumento de armadilhas extracelulares de neutrófilos (NETs). Esses ácidos de DNA/RNA livres de células ativam as vias de sinalização acima através de sensores intracelulares de DNA/RNA para desencadear a produção de IFN-I (90). Estudos mostraram que existem vários loci gênicos de suscetibilidade relacionados ao LES nas vias de sinalização acima, e suas variantes gênicas contribuem para a produção de IFN-I e a progressão de LN (Tabela 1).
Os principais produtores de IFN-I no rim
O sistema IFN-I no LES está em um estado de ativação de longo prazo. Todos os tipos de células nucleadas podem produzir IFN-I durante a infecção patogênica. Sob o pano de fundo do LES, as células imunes são anormalmente ativadas. Por exemplo, células dendríticas plasmocitóides (pDCs) produzem massivamente IFN-a (103); os neutrófilos secretam IFN-I nos estágios iniciais da doença (104). As células B T1 precoces no LES produzem IFN-I, especialmente IFN-b (105). Um estudo anterior mostrou que as células residentes renais (em vez de células imunes infiltrantes) eram a principal fonte de IFN-I norim(80). Além do ácido nucleico livre de células circulantes e do componente de ácido nucleico dos CICs, os ácidos nucleicos imunoestimuladores renais são uma fonte importante de ácido nucleico patogênico. Grandes fragmentos de cromatina norimsão expostos devido à regulação seletiva para baixo da atividade de Dnase1 no rim (16, 106, 107). Os autoanticorpos nefrogênicos do lúpus entram nas células renais, danificando a estrutura celular, aumentando a clivagem do DNA e induzindo a morte celular (29, 108). Outra fonte potencial de ácidos nucleicos imunoestimuladores renais são os NETs liberados por neutrófilos no glomérulo e túbulo renal, que não são totalmente degradados e são feitos de DNA, histonas e proteínas de neutrófilos (109-111). NETs ativam a via cGAS-STING ou a via TLR9 para produzir IFN-I (111, 112). O subtipo de IFN-I secretado pelas células residentes renais e a expressão de receptores de DNA/RNA nas células renais variou (Tabela 2).
Podócito
DNA/RNA-ICs induzem a produção de IFN-b em podócitos. Podócitos tratados com ligante de TLR3 - poliIC - expressaram IFN-I. E os podócitos expressam TLR1-6 e TLR9 (113). Masum MA et ai. descobriram que TLR9 é superexpresso em podócitos em camundongos com glomerulonefrite autoimune (AGN), que está associada à lesão glomerular de podócitos (114). No entanto, Machida H et al. descobriram que TLR9 foi expresso apenas em podócitos de pacientes com LN ativos e desapareceu durante a remissão (115). cGAS e IFI16 são os principais sensores de DNA em podócitos e desencadeiam a expressão de IFN-b ativando a via cGAS/IFI16-STING, promovendo assim a progressão de LN em pacientes com LES (116). Além disso, Kimura J et al. analisaram camundongos modelo de lúpus BXSB/MPJ-YAa e descobriram que a expressão de TLR8 e suas citocinas a jusante foi significativamente aumentada em camundongos lúpicos, e TLR8 foi localizado em podócitos (117).
RMC
DNA/RNA-ICs induzem a produção de IFN-b em RMCs. No contexto do LES, os RMCs expressam TLR1-4 e TLR6, especialmente TLR3 de alta expressão (118). TLR3 pertence ao subgrupo TLR específico de ácido nucleico que ativa a produção de IFN-b reconhecendo dsRNA (119). No entanto, os RMCs não expressam outros membros do subgrupo TLR — TLR{10}} (118, 119). Além disso, os RMCs de pacientes com NL apresentam altos níveis de expressão de MDA5 (120). dsRNA induz RMCs a liberar IFN-a/b por MDA5 (em vez de RIG-I); IFN-a/b pode ativar RMCs em um loop autócrino-parácrino (121). Embora os RMCs não expressem TLR9 (118, 119), os DNA-ICs também induzem a ativação de RMCs. Qing X et ai. descobriram que anticorpos anti-dsDNA IgG regulam positivamente os genes pró-inflamatórios de RMCs em camundongos MRL/LPR (122). Allam R et ai. descobriram que o dsDNA viral estimulou RMCs a produzir genes induzidos por IFN-b e IFN que são independentes de DAI (123).

GEC
DNA/RNA-ICs induzem a produção de IFN-b em GECs. GECs expressam TLR1-6 (124). dsRNA ativa TLR3 e induz GECs a expressar IFN-b (125, 126). Liu Q et ai. descobriram que o dsRNA induziu a expressão de GECs de RIG-I e MDA5 através da via de sinalização TLR3/IFN-b (127). Ao mesmo tempo, o dsRNA ativa GECs através de RIG-I para secretar IFN-a/b, enquanto IFN-a/b não pode ativar GECs em uma alça autócrina-parácrina (128). Os GECs não possuem um TLR específico de DNA exclusivo - TLR9 (124). No entanto, Hagele H et al. estimularam GECs com dsDNA viral e descobriram que o dsDNA viral entrou em GECs por endocitose e, em seguida, ativou GECs para produzir IFN-a/b de maneira independente de TLR (129). O IFN-b pode induzir a expressão de DAI e a fosforilação de IRF3, mas o IFN-b não pode ativar GECs em uma alça autócrina-parácrina (129).
Outros
As células renais residentes também incluem TECs, fibroblastos intersticiais renais e células endoteliais capilares peritubulares (ECs PTC). Castellano G et ai. descobriram que a TEC era o principal produtor de IFN-a (130). Estudos recentes descobriram que os TECs expressam RIG-I, um receptor de reconhecimento de padrão intracelular que participa da produção de IFN-b reconhecendo RNA (131). Não se sabe se os fibroblastos intersticiais renais produzem IFN-I e sua expressão de receptor de DNA/RNA intracelular. O nível de expressão de TLR9 foi significativamente aumentado em CEs de PTC em camundongos modelo AGN propensos ao lúpus e foi associado a lesão intersticial tubular renal e capilar peritubular (132).
OS EFEITOS DE DANOS DO IFN-I NO LN
As células renais são a principal fonte de IFN-I norim(80). O IFN-I induzido por células residentes renais, por sua vez, promove o estado inflamatório das células glomerulares, levando àfibrose, cicatrizes e perda renal (80). O dano do IFN-I se manifesta em três aspectos: (1) o IFN-I induz a produção de antígeno nuclear e autoanticorpos, promovendo a formação de CIs; (2) IFN-I recruta leucócitos para promover lesões proliferativas; (3) O IFN-I atua nas células renais residentes, levando à ativação celular, lesão, apoptose e progressão para insuficiência renal.fibrose(Figura 4).
IFN-I Promove a Formação de Antígenos Nucleares e Autoanticorpos
O IFN-I promove a formação de antígenos nucleares. IFN-I pode induzir a expressão e mobilização do fator de ativação de células B (BAFF) (133, 134). BAFF promove a ativação de células T (135) e a produção de NETs (136). A hiperatividade das células T do LES leva à hiperpolarização mitocondrial, que em última análise leva ao aumento da produção de espécies reativas de oxigênio (ROS) (137). ROS podem modificar componentes celulares e metabólitos, dando-lhes imunogenicidade (138). ROS contribui para a formação de NETs (112). Os NETs desencadeiam uma ativação concertada de TLR9 e receptor de células B (BCR) levando à produção de autoanticorpos no lúpus (139). Células T auxiliares foliculares (TFHs) (140, 141), CXCR5-CXCR3 mais PD1hiCD4 mais células T auxiliares (142) e células T auxiliares periféricas (TPHs) (143) promovem a diferenciação de células B e a produção de anticorpos em diferentes caminhos.
O IFN-I promove a formação de autoanticorpos. BAFF é um fator chave na maturação, sobrevivência e função das células B patogênicas do LES (144, 145), que são responsáveis pela produção de autoanticorpos. O IFN-I não apenas mobilizou diretamente o BAFF (133, 134), mas também regulou indiretamente a via do BAFF, promovendo a produção de fatores inibitórios de macrófagos (MIF) (146-148). BAFF também promove a ativação de células B por IFN (149). Além disso, autoanticorpos e CIs relacionados ao LES podem induzir a forte liberação de NETs (150), aumentando a exposição ao ácido nucleico.
Em seguida, o aumento de antígenos nucleares e autoanticorpos induzidos por IFN-I aumentam a chance de formação de IC e desencadeiam LN.
IFN-I Promove a Infiltração de Leucócitos
O IFN-I induz fortemente a quimiocina CXCL9/10/11, então recruta leucócitos para o sítio inflamatório através da via de sinalização CXCR3A-Gi PI3K-MAPK (151, 152). Vários estudos descobriram que o IFN-I renal induziu leucócitos no rim em pacientes com NL. O aumento do recrutamento de leucócitos pode ser um mecanismo operatório que o IFN-I leva à nefrite imunomediada (80). Triantafyllopoulou A et al. induziu a superexpressão de IFN-b em camundongos NZB/W usando o ligante poli de TLR3 (I: C) e descobriu que o IFN-b induziu infiltração macrofágica no tecido renal (78). Yoshikawa M et ai. descobriram que IFN-b regula negativamente a expressão de CXCR5 em células B e IFN-g regula positivamente a expressão de CXCR3 em células B, o que induz a infiltração de células B no tecido renal de pacientes com NL (153). Além disso, o IFN-I regula essas células imunes. Kishimoto D et ai. descobriram que o IFN-I inibiu as propriedades anti-inflamatórias de macrófagos do tipo M2-no glomérulo pela regulação positiva de Bach1 e regulação negativa da expressão de ho-1, promovendo assim a inflamação glomerular (154).

IFN-I Promove Lesão do Tecido Renal
IFN-I Promove Esclerose Glomerular
Podócito
O comprometimento da estrutura podocitária é um dos primeiros sintomas da lesão glomerular e é uma característica da NL (155-157). Os podócitos são células epiteliais altamente diferenciadas que são fixadas na membrana basal através da extensão do processo do pé e interagem com os podócitos circundantes para formar um diafragma em fenda e, eventualmente, uma barreira de filtração. O diafragma de fenda é uma conexão celular única formada por proteínas específicas de podocina, como nefrina e podocina, que interagem com o citoesqueleto de actina (158). O citoesqueleto de actina é a estrutura principal dos podócitos. Distúrbios do citoesqueleto de actina desempenham um papel importante na FPE e na catástrofe mitótica, levando ao descolamento de podócitos e proteinúria (159-161).
As células podócitos são induzidas a produzir IFN-b, que por sua vez estimula a expressão podócito B7-1 e a remodelação da actina (162). O IFN-b promove especificamente o descolamento ou morte de podócitos por indução de catástrofe mitótica em podócitos. O IFN-a previne o reparo de podócitos causando parada do ciclo celular e inibindo a proliferação e migração de PECs. E ambos os IFNs acima suprimem a diferenciação do progenitor renal em podócitos maduros, que são propícios à formação de cicatriz focal, mas não ao reparo glomerular (163). dsDNA induz podócitos a secretar IFN-b. A expressão de IFN-b ativa o IFNAR. As quinases JAK1 e TYK2 associadas ao IFNAR então fosforilam STAT1, que promove a transcrição da apolipoproteína L1 (APOL1). E o STAT1 ativado regula positivamente o IFI16, que aciona um mecanismo de feedback positivo que promove a expressão do APOL1 (116). A superexpressão de APOL1 em podócitos é altamente tóxica. Os alelos APOL1 G1 e G2 são fatores de risco para NL e doença renal terminal associada adoença de Lupus(LN-ESRD) em afro-americanos (164, 165). A lesão observada de podócitos glomerulares em LN sugere que o aumento da variante de risco APOL1 em podócitos de pacientes com LES pode promover a progressão mais rápida de LN e LN-ESRD (155-157). Estudos recentes mostraram que o IFN-a também está associado a danos na estrutura e função dos podócitos. O IFN-a tem um efeito significativo na função de barreira de filtração dos podócitos. Ao mesmo tempo, o IFN-a atenua o sinal mTORC1 e induz a autofagia dos podócitos. No entanto, o aumento da autofagia melhora a lesão podocitária induzida por IFN-a (166). Isso parece mostrar uma regulação protetora de feedback negativo.
GEC
GECs também são o componente da barreira de filtração glomerular. Estudos anteriores mostraram que o IFN-I, especialmente o IFN-a, mediava a disfunção endotelial e causava a apoptose das CE (167), o que aumenta a permeabilidade dos GECs e resulta em uma perda da função de barreira de filtração glomerular.
RMC
RMCs são o fator chave no LN glomerularfibroseem L.N. Eles desempenham um papel importante na homeostase, mantendo a estrutura glomerular, produzindo e mantendo a matriz mesangial, regulando a área de superfície de filtração e fagocitando células apoptóticas ou CIs (49). Em resposta à deposição de CIs e lesão induzida por citocinas, as RMCs promovemfibrosepor hipertrofia e proliferação (168). PDGF-B é um fator de crescimento indutor de proliferação/migração que induz a proliferação de RMC na glomerulonefrite (169). TGF-b1 ativa a via de sinalização Smads a jusante por autócrina/parácrina, induzindo a produção de PDGF-B. A alça autócrina/parácrina de IFN-b ativa Smad7 que inibe a ativação de Smad3/4 e previne a indução de PDGF-B (170). No entanto, estudos mostraram que a estimulação de IFN-a/b aumenta a expressão de TGF-b1 (44, 78), o que pode aumentar a expressão de PDGF-B e promover a proliferação de RMCs. Além disso, CXCL10 induzida por IFN-I não só recruta leucócitos, mas também agrava a proliferação de RMC ativando a via de sinalização ERK (171).
Além da proliferação excessiva, as RMCs são uma das principais células geradoras de estroma, secretando componentes da matriz mesangial, como colágeno tipo I (COL I), colágeno tipo III (COL III) e fibronectina (FN). A via de sinalização TGF-b1/Smads desempenha um papel importante no excesso de matriz extracelular (ECM) (172, 173). Primeiro, a via de sinalização TGF-b1/Smad regulou positivamente a síntese de proteínas da matriz, incluindo COL I e COL III. Em segundo lugar, a via de sinalização TGF-b1/Smad inibe a degradação da matriz. A adição de TGF-b1 ao glomérulo normal reduziu significativamente a atividade do ativador do plasminogênio (PA) e aumentou a síntese do inibidor do ativador do plasminogênio 1 (PAI-1) (174). TGF-b1 regula a expressão de MMP-9 (44); a principal função das MMPs é degradar os componentes da ECM, então parece que o TGF-b1 aumenta a degradação da matriz. No entanto, um grande número de estudos mostrou que os níveis de MMPs e inibidores teciduais de metaloproteinases (TIMPs) no soro, urina e glomérulo de pacientes com NL estão aumentados, acompanhados pela deposição da matriz mesangial (78, 175-179) . MMPs superexpressas interagem com TIMPs, alterando a composição da matriz para promover a expansão da matriz mesangial (178). IFN-a/b induz alta expressão de MMP-9 e TIMP-1 no rim (78). Além disso, o TGF-b1 altera a expressão das integrinas mesangiais a1b1 e a5b1 e seus ligantes (como laminina, colágeno e FN), promovendo adesão à matriz (180).
O IFN-I pode induzir indiretamente a expressão de TGF-b1 em RMCs. Além de CXCL10, IFN-I induziu a expressão de RMCs de proteínas de quimiotaxia de monócitos 1(MCP-1/CCL2) e IL6. Níveis aumentados de MCP-1 estimulam a formação de TGF-b1 em células residentes renais (181) e induzem a expressão de mRNA de Col IV, deposição de colágeno e expressão de FN (182). O papel da IL-6 na função renalfibrosepermanece controverso. Estudos anteriores mostraram que IL-6 não desempenha um papel importante no desenvolvimento de doenças renaisfibrose(183). Estudos recentes mostraram que a superexpressão de IL-6 e seu receptor reduz a abundância de FN e Col IV em RMCs (184); A transdução de sinal trans de IL-6 pode estar envolvida na ocorrência e desenvolvimento de fibrose renal (185). Isso é consistente com a teoria de que a sinalização de IL-6 é mediada por duas vias principais. A atividade anti-inflamatória de IL-6 é mediada por vias de sinalização clássicas, enquanto a propriedade pró-inflamatória é mediada por vias de sinalização trans (186). Além disso, as alças autócrinas/parácrinas de IFN-I induzem em grande parte a morte de RMCs (121). No geral, o IFN-I mostra um efeito prejudicial significativo nos RMCs (187, 188).
IFN-I Promove Fibrose Intersticial Renal
Intersticial renalfibroseé o resultado do processo inflamatório crônico. Durante a inflamação crônica, diferentes componentes celulares e redes de sinalização complexas interagem para levar ao desenvolvimento de miofibroblastos renais, que levam ao acúmulo excessivo de MEC, uma característica importante e comum de diferentes doenças renais crônicas. A possível origem dos miofibroblastos de células epiteliais/endoteliais renais, fibroblastos ou pericitos permanece um assunto de debate (189-195). LeBleu VS et al. mostraram que 50% dos miofibroblastos proliferativos são derivados de fibroblastos residentes; miofibroblastos não proliferativos derivam através da diferenciação da medula óssea (35 por cento), o programa de transição endotelial-mesenquimal (EndMT) (10 por cento) e o programa de transição epitelial-mesenquimal (EMT) (5 por cento) (193) . TGF-b1 ainda desempenha um papel central em muitos fatores fibróticos (196). Primeiro, o TGF-b1 promove a proliferação de fibroblastos. O fator de crescimento de fibroblastos 2 (FGF-2) é um poderoso mitógeno de fibroblastos, promovendo o crescimento autócrino de fibroblastos (197). TGF-b1, PDGF-B e FGF-2 promovem conjuntamente a proliferação de fibroblastos (197-199). Em segundo lugar, o TGF-b1 promove a transformação de outras células em miofibroblastos. TGF-b1 induz a transformação funcional de TECs e GECs em miofibroblastos, que são responsáveis pela deposição de ECM (193, 200-204). MMP-9 está envolvido em EndMT e EMT através da regulação ascendente da sinalização Notch, e sua ativação está localizada a jusante de TGF-b1 (205, 206). FGF-2 também desempenha um papel importante na EMT (207–209). TGF-b1 também está envolvido na transformação de fibroblastos-miofibroblastos através da fosforilação de TGFR1 e subsequente via Smad2/3 mediando a transcrição de a-SMA e diferenciação de miofibroblastos (210). TGF-b1 e PDGF transformam fibroblastos em miofibroblastos (211, 212), que junto com fibroblastos produzem ECM (213, 214). Além da via de sinalização de TGF-b1, a sinalização de PDGF induz a proliferação e diferenciação de pericitos em miofibroblastos (64, 215-218). Além disso, TGF-b1 regula PA, PAI-1, MMP-9 e integrina para inibir a degradação da matriz e promover o acúmulo de ECM e intersticialfibrose(44, 174, 178, 180).
TGF-b1 é produzido principalmente por TECs. Se IFN-I induz TECs a secretar TGF-b1 continua a ser visto. IFN-a induz instabilidade de barreira e apoptose de TECs (219-221), que podem ativar TECs. Nos recentes estudos de sequenciamento de RNA de célula única de biópsias renais de pacientes com NL, a expressão de genes de resposta a IFN-I em TECs de pacientes com NL foi significativamente maior do que a de indivíduos controles saudáveis (222) e se correlaciona com os escores clínicos e com a resposta ao tratamento (223). Os TECs ativados secretam uma série de mediadores pró-inflamatórios e absorvem mais monócitos circulantes no tubulointerstício renal; monócitos infiltrados tornam-se macrófagos ativados (224). IFN-I também recrutou macrófagos para se infiltrar (78). Macrófagos ativados secretam PDGF, TGF-b1, MMP e TIMP, que estão envolvidos na regulação do tecidofibrose(224). Da mesma forma, IFN-I pode melhorar o processo de intersticial renalfibroseatravés de MCP-1/CCl2 e IL-6 (181, 184, 185).
IFN-I Promove Lesões Microvasculares Renais
O desequilíbrio entre lesão e reparo endotelial vascular é um evento chave nas lesões vasculares. IFN-I quebra esse equilíbrio (225). As células progenitoras endoteliais (EPCs) são o principal mecanismo de reparo. O IFN-I induz a expressão de CXCL9/10/11. CXCL9/10/11 ativa as vias de sinalização do receptor de quimiocina-3B (CXCR3B)-Gs-adenilil ciclase (AC)-monofosfato de adenosina cíclico (cAMP)-proteína quinase A (PKA), promovendo diretamente a disfunção de ECs e EPCs ( 225). Também regula positivamente a função de outros fatores de disfunção pró-EPC (IL-18 (226), BAFF (133, 134, 227)) e regula negativamente a função de moléculas pró-angiogênicas (IL{{26 }}b e VEGF (167)), que indiretamente leva à disfunção EPC.
O IFN-I promove a imperfeição vascular afetando os pericitos. IFN-I regula a expressão de TGF-b1 e PDGF (44, 78, 170). As vias de sinalização de TGF-b1 e PDGF induzem pericitos a proliferar e diferenciar em miofibroblastos (64, 215-218). Os pericitos estão ligados à superfície da parede capilar e compartilham uma origem de desenvolvimento com os fibroblastos. Os pericitos normais estabilizam as paredes dos vasos sanguíneos e mantêm a tranquilidade e a integridade dos vasos. Pericitos ativados são liberados da parede vascular e transformados em miofibroblastos (195, 228-232). A perda de pericitos leva à formação de capilares frágeis e vasos sanguíneos instáveis e patológicos, resultando em afinamento vascular renal (233). A perda de capilares ao redor dos túbulos renais está intimamente relacionada àfibrose.
CONCLUSÃO
O acúmulo de DNA/RNA livre de células é o passo inicial do lúpus e da NL. O DNA/RNA livre de células e os componentes de ácido nucleico dos CIs acionam os sensores de DNA/RNA nas células residentes renais, ativando assim a via de sinalização para a produção de IFN-I. O IFN-I, por sua vez, induz a exposição ao ácido nucleico e a formação de autoanticorpos. O IFN-I atua nas células residentes renais e está envolvido em todo o processo de lesão renal, principalmente na ativação da via de sinalização TGF-b1/Smads. Além disso, o IFN-I recruta leucócitos para os tecidos renais através da via de sinalização CXCL9/10/11- CXCR3A-Gi-PI3K-MAPK, aumentandofibroseresposta. Além disso, o IFN-I promove lesões microvasculares renais, prejudicando ainda mais a função renal. O IFN-I é encontrado em quase todos os elos da patogênese da NL. Portanto, o IFN-I desempenha um papel importante na patogênese da NL. O direcionamento de sistemas IFN-I no rim tem efeitos terapêuticos potenciais no surgimento prematuro de LN em pacientes com LES. Também sugere que a função imune das células renais residentes é maior do que a das células renais imunes em LN e as células renais residentes são o jogador dominante e aceptor na ocorrência e desenvolvimento de LN. O estudo sobre células residentes renais aprofundará ainda mais a compreensão da NL e contribuirá para a terapia direcionada da NL no futuro.

CONTRIBUIÇÕES DO AUTOR
XD e YR fizeram a pesquisa bibliográfica e redigiram o artigo. XH deu uma visão. XH revisou o artigo. Todos os autores contribuíram para o artigo e aprovaram a versão submetida.
FINANCIAMENTO
Este trabalho foi apoiado pela Fundação Nacional de Ciências Naturais da China (No. 61562021 e No. 81560275, No. 81960885, No. 81260139, No. 81060073, No. 30560161), Hainan Major Science and Technology Projects (ZDKJ2039010), Hainan Association para a excelência acadêmica Programa de Inovação em Ciência e Tecnologia da Juventude (201515), projetos especiais de Hainan de Desenvolvimento Social (ZDYF2018103 e 2015SF39).
AGRADECIMENTOS
Os autores agradeceram a Xiayang Chen por revisar e revisar este artigo.
REFERÊNCIAS
1. Almaani S, Meara A, Rovin BH. Atualizar emDoença de Lupus. Clin J Am Soc Nephrol (2017) 12:825–35.
2. Hanly JG, O'Keeffe AG, Su L, Urowitz MB, Romero-Diaz J, Gordon C, et al. A frequência e o resultado da nefrite lúpica: resultados de um estudo de coorte internacional. Reumatol (Oxford) (2016) 55:252–62.
3. Parikh SV, Almaani S, Brodsky S, Rovin BH. Atualizar emDoença de Lupus: Currículo Básico 2020. Am J Kidney Dis (2020) 76:265–81.
4. Maningding E, Dall'Era M, Trupin L, Murphy LB, Yazdany J. Diferenças raciais e étnicas na prevalência e tempo de início das manifestações de lúpus eritematoso sistêmico: o projeto de vigilância do lúpus da Califórnia. Arthritis Care Res (Hoboken) (2020) 72:622–9.
5. Pinheiro S, Dias RF, Fabiano R, Araujo SA, Silva A. PediatriaDoença de Lupus. J Bras Nefrol (2019) 41:252–65. doi
6. Yap DY, Tang CS, Ma MK, Lam MF, Chan TM. Análise de Sobrevivência e Causas de Mortalidade em Pacientes com Nefrite Lúpica. Transplante Nephrol Dial (2012) 27:3248–54.
7. Tektonidou MG, Dasgupta A, Ward MM. Risco de doença renal terminal em pacientes comDoença de Lupus, 1971-2015: Uma Revisão Sistemática e Meta-Análise Bayesiana. Artrite reumatol (2016) 68:1432-41.
8. FaurschouM,DreyerL,KamperAL, StarklintH,JacobsenS. Mortalidade a longo prazo e desfecho renal em uma coorte de 100 pacientes comDoença de Lupus. Arthritis Care Res (Hoboken) (2010) 62:873–80.
9. Lerang K, Gilboe IM, Steinar TD, Gran JT. Mortalidade e anos de vida potencial perdidos no lúpus eritematoso sistêmico: um estudo de coorte de base populacional. Lúpus (2014) 23:1546-52. doi:
10. Bernatsky S, Boivin JF, Joseph L, Manzi S, Ginzler E, Gladman DD, et al. Mortalidade no Lúpus Eritematoso Sistêmico. Arthritis Rheum (2006) 54:2550–7.
11. Furie R, Rovin BH, Houssiau F, Malvar A, Teng Y, Contreras G, et al. Ensaio de dois anos, randomizado e controlado de Belimumab na nefrite lúpica. N Engl J Med (2020) 383:1117–28.
12. Zhang H, Zhou M, Han X, Yang Y, Yu X. Micofenolato de mofetil no tratamento de pacientes chineses comDoença de Lupus: Metanálise compatível com APRISMA. Med (Baltimore) (2020) 99:e21121.
13. Yung S, Chan TM. Autoanticorpos e células renais residentes na patogênese daDoença de Lupus: Conhecendo o Desconhecido. Clin Dev Immunol (2012) 2012:139365.
14. Lech M, Anders HJ. A Patogênese daDoença de Lupus. J Am Soc Nephrol(2013) 24:1357–66.
15. Mortensen ES, Rekvig OP. Potencial Nefritogênico de Anticorpos Anti-DNA Contra Nucleossomos Necróticos. J Am Soc Nephrol (2009) 20:696–704.
16. Fismen S, Mortensen ES, Rekvig OP. Deficiências de Nuclease promovem o estágio finalDoença de LupusMas não autoimunidade nefritogênica em camundongos (NZB × NZW) F1. Immunol Cell Biol (2011) 89:90 - 9.
17. Yung S, Chan TM. Anticorpos Anti-Dsdna e Células Renais Residentes - Seus Papéis Supostos na Patogênese de Lesões Renais emDoença de Lupus. Clin Immunol (2017) 185:40–50.
18. Lim EJ, Lee SH, Lee JG, Kim JR, Yun SS, Baek SH, et al. Receptor Toll-Like 9 A ativação dependente de MAPK e NF-Kb é necessária para a expressão de matriz metaloproteinase -9 induzida por Cpgodn. Exp Mol Med (2007) 39:239–45.
19. Merrell MA, Ilvesaro JM, Lehtonen N, Sorsa T, Gehrs B, Rosenthal E, et al. Os agonistas do receptor 9 Toll-Like promovem a invasão celular aumentando a atividade da metaloproteinase da matriz. Mol Cancer Res (2006) 4:437-47.
20. CM geral. Determinantes Moleculares da Especificidade do Substrato de Metaloproteinase: Domínios, Módulos e Exosítios de Ligação do Substrato de Matrixmetaloproteinase. Mol Biotechnol (2002) 22:51–86.
