Compreendendo o comprometimento renal e as malignidades de órgãos sólidos e gerenciando o câncer renal
Feb 27, 2022
Contato: emily.li@wecistanche.com
Camilo Porta, et al.
A associação entrerimdoençae o câncer é multifacetado e complexo. Pessoas com doenças crônicasrimdoença(DRC) têm uma incidência aumentada de câncer, e tanto o câncer quanto os tratamentos contra o câncer podem causar comprometimento da função renal. Problemas renais no cenário de malignidade podem piorar os resultados dos pacientes e diminuir a adequação dos tratamentos anticâncer. Além disso, o cenário do tratamento oncológico está mudando rapidamente, e muitas vezes faltam dados sobre a tolerabilidade de novas terapias em pacientes com DRC. O atendimento ao paciente oncológico tornou-se mais especializado e interdisciplinar, exigindo atualmente a colaboração de especialistas em nefrologia, oncologia médica, cuidados intensivos, farmacologia clínica/farmácia e cuidados paliativos, além de cirurgiões e urologistas. Para identificar os principais problemas de gerenciamento em nefrologia relevantes para pacientes com malignidade, KDIGO(RimDoença: Improving Global Outcomes) reuniu um painel global de especialistas clínicos e científicos multidisciplinares para uma conferência de controvérsias sobre conefrologia em dezembro de 2018. Este relatório abrange questões relacionadas ao comprometimento renal e malignidades de órgãos sólidos, bem como ao gerenciamento e tratamento do câncer renal. As lacunas de conhecimento, áreas de controvérsia e prioridades de pesquisa são descritas.
PALAVRAS-CHAVE:Taxa de filtração glomerular; nefrotoxicidade; oncologia; carcinoma de células renais

Cistanche é bom para doença renal
Rimdoençae câncer têm uma associação multifacetada. Pessoas com doenças crônicasrimdoença(DRC) têm uma incidência aumentada de câncer em relação aos pacientes sem DRC.1,2 Além disso, tanto o câncer quanto os tratamentos contra o câncer podem causarrimfunção, incluindo agudarimprejuízo(IRA) ou DRC. Problemas renais no cenário de malignidade podem piorar os resultados dos pacientes e diminuir a adequação dos tratamentos anticâncer. Pacientes cujo câncer é potencialmente curável podem apresentar falência de múltiplos órgãos, exigindo cuidados intensivos e terapia de substituição renal. Em alguns países, a melhora da mortalidade por câncer causada pela maior eficácia do tratamento resultou em uma população crescente de sobreviventes de câncer3 que correm maior risco derimdoença. Finalmente, a malignidade avançada complicada por doença multiorgânica levanta questões relacionadas à adequação do tratamento agressivo versus terapia paliativa.
A complexa relação entrerimdoençae o câncer é confundido por um cenário de tratamento em rápida mudança. O atendimento ao paciente oncológico tornou-se mais especializado e interdisciplinar, exigindo atualmente a colaboração de especialistas em nefrologia, oncologia médica, cuidados intensivos, farmacologia clínica/farmácia e cuidados paliativos, além de cirurgiões e urologistas. Para identificar os principais problemas de gerenciamento em nefrologia relevantes para pacientes com malignidade, o KDIGO (Kidney Disease: Improving GlobalOutcomes) reuniu um painel global de especialistas clínicos e científicos multidisciplinares para uma conferência de controvérsias sobre onco-nefrologia em Milão, Itália, em dezembro de 2018. Este relatório abrange questões relacionadas comrimimparidadee malignidades de órgãos sólidos, bem como a gestão e tratamento do cancro do rim. As lacunas de conhecimento, áreas de controvérsia e prioridades para pesquisa são descritas.
DEFICIÊNCIA RENAL E MALIGNIDADES DE ÓRGÃOS SÓLIDOS
A DRC é altamente prevalente em pacientes com câncer; a prevalência da taxa de filtrado glomerular estimada (eGFR)<60 ml/min="" per 1.73="" m2 in="" cancer="" patients="" is="" estimated="" to="" be="" 12%="" to="" 25%.4–9 certain="" cancers,="" such="" as="" renal="" cell="" carcinoma="" (rcc)7,10 and bladder="" cancer,11 have="" a="" higher="" prevalence="" of="" ckd="" than others.="" the="" presence="" of="" ckd="" worsens="" the="" survival="" rates="" of cancer="" patients.5,8,12–14 patients="" with="" ckd="" g5="" are="" at="" a="" higher risk="" of="" certain="" types="" of="" cancers:="" kidney,="" bladder,="" and="" infection-associated="" cancers="" such="" as="" tongue,="" liver,="" and="" cervix.15–19 in men,="" ckd="" g3="" or="" higher="" has="" been="" associated="" with="" an="" elevated risk="" of="" urinary="" tract="" cancers.20 it="" is="" unknown="" why="" patients with="" ckd="" have="" increased="" cancer-related="" mortality="" relative to="" those="" who="" do="" not="" have="" ckd="" (table="">

As causas e mecanismos fisiopatológicos de LRA e DRC em cânceres sólidos são pré-renais (por exemplo, depleção de volume, hipotensão, compressão vascular, caquexia do câncer), renais (por exemplo, doenças glomerulares, doença tubulointersticial, doença renovascular) e pós-renais (por exemplo, obstrução volumosa, retenção urinária, nefrolitíase).

Avaliação derimfunçãoA medição precisa da TFG é crucial ao decidir sobre o tratamento e a dosagem do medicamento e o monitoramentorimfunção. Infelizmente, todas as fórmulas disponíveis podem subestimar ou superestimar a TFG.25 Além disso, a presença de sarcopenia causa imprecisões na estimativa da TFG. Diferentes equações baseadas em creatinina são usadas para estimar a TFG no câncer: a fórmula de Cockcroft-Gault, a equação do estudo Modificação da Dieta na Doença Renal e a equação da Colaboração em Epidemiologia da Doença Renal Crônica (CKD-EPI). No entanto, esses modelos para estimativa da TFG foram desenvolvidos principalmente em populações não cancerosas, e sua utilidade em contextos oncológicos é incerta. Recentemente, um grande estudo de Janowitz et al. demonstraram que a equação CKD EPI ajustada para a área de superfície corporal foi o estimador mais preciso e menos tendencioso da TFG em pacientes com câncer, com base em uma comparação com a depuração radioisotópica com ácido cromo-51 etilenodiaminotetracético.26
O grupo de trabalho da conferência concordou que a equação CKD-EPI27 é a melhor abordagem atual para a dosagem de agentes quimioterápicos em pacientes com DRC. O uso de equações baseadas na cistatina C pode conferir melhor acurácia na predição da eliminação de drogas pelos rins28; no entanto, com tratamentos oncológicos direcionados, a proteólise mediada por catepsina D pode diminuir a cistatina C, independentemente darimfunção. Portanto, o uso universal de equações baseadas em cistatina C não é recomendado.29 O uso da fórmula de Cockcroft-Gault para determinar a dosagem de agentes quimioterápicos é problemático porque pode subestimar a depuração de creatinina, levando a reduções inadequadas de dose de tratamentos contra o câncer.30 Melhores métodos para estimar a TFG são necessários, assim como testes no local de atendimento que podem medir rapidamente a TFG.31,32
Aplicabilidade e eficácia de vários diagnósticos no cenário da onco-nefrologia
Investigações renais em pacientes com neoplasias de órgãos sólidos. Para pacientes com malignidade de órgãos sólidos, as principais investigações renais no momento do diagnóstico são a avaliação derimfunção, comorbidades, equilíbrio ácido-base e eletrólitos, bem como análise de urina. A ultrassonografia renal é útil em pacientes com câncer que desenvolvem IRA, a menos que os rins já tenham sido avaliados adequadamente com outras imagens radiológicas. Em candidatos à nefrectomia, a cintilografia renal pode ser usada para avaliar orimfunção, ou pode apoiar a escolha de cirurgia radical versus parcial com CCR. Durante o tratamento oncológico, para pacientes com ou sem LRA, as investigações renais incluiriam os exames usuais de acompanhamento com base no tipo de câncer e nas terapias. Para pacientes em que a LRA está se desenvolvendo (Tabela Suplementar S1),33 as principais avaliações renais são semelhantes às sugeridas no diagnóstico de câncer, com a adição da relação proteína-creatinina da urina spot. Durante o acompanhamento após o tratamento oncológico, as consultas de nefrologia são indicadas se os pacientes apresentarem alterações na função renal ou aumento da proteinúria.
Rastreamento de câncer em pacientes em diálise.
Triagem do câncer no cenário derimfalhapode ser custo-efetivo se a sobrevida esperada for longa o suficiente ou se o paciente for um candidato a transplante. Por outro lado, o rastreamento abrangente em pacientes com expectativa de vida limitada pode não ser benéfico.34 Portanto, as decisões sobre o rastreamento do câncer em pacientes com DRC G5 devem ser tomadas individualmente, levando em consideração a sobrevida esperada, os fatores de risco e o status do transplante.
Rastreamento de câncer em pacientes com glomerulonefrite.
All patients with membranous nephropathy, particularly those older than 60 years, should be considered for cancer screening following age-appropriate guidelines. Patients with membranous nephropathy who have features of secondary membranous nephropathy on kidney biopsy (subendothelial or mesangial deposits, >8 glóbulos brancos por glomérulo, subtipo não-IgG-4) devem ser rastreados mais intensamente para malignidade subjacente.35 Pacientes com doença de lesão mínima que apresentam anemia inexplicada, eletroforese anormal de proteínas séricas, hepatoesplenomegalia ou linfadenopatia também devem ser rastreados para malignidade subjacente, especialmente linfoma de Hodgkin.36
Biópsia renal em pacientes com câncer com anormalidades urinárias.
Kidney biopsy should be considered in cancer patients with significant new-onset proteinuria (defined as >1 g/d pelos participantes da conferência) ou piora da função renal quando o diagnóstico derimdoençanão pode ser estabelecido de outra forma e pode alterar a gestão do cuidado. A biópsia renal não deve ser realizada em pacientes com câncer com prognóstico reservado; se o ganho esperado para um diagnóstico apropriado for menor que a sobrevida esperada do paciente, é improvável que uma biópsia seja útil.
Em pacientes com câncer renal submetidos à cirurgia, o exame de tecido renal não neoplásico é altamente recomendado para identificar doenças do parênquima renal coexistentes.37,38 A indicação de biópsia renal em sobreviventes de câncer, sem câncer ativo e bom prognóstico, deve ser semelhante às diretrizes da população geral. No entanto, a biópsia e, eventualmente, a rebiópsia podem ser consideradas para avaliar as consequências a longo prazo da terapia sistemática e da toxicidade renal induzida por radiação.38,39
Até o momento, poucas biópsias estão sendo realizadas em pacientes com câncer com complicações renais. De fato, um biobanco de amostras de rim ou um registro internacional de biópsia pode ser útil para entender o espectro da doença e os resultados (Tabela 1).

Prevenir o desenvolvimento ou progressão de LRA ou DRC
Inibidores da Enzima Conversora da Angiotensina ou Bloqueadores do Receptor da Angiotensina II em Pacientes com DRC ou câncer nefrectomizado.
Inibidores da enzima conversora da angiotensina (ECA) ou bloqueadores dos receptores da angiotensina II (BRAs) devem ser considerados em pacientes nefrectomizados com DRC nos quais há indicação clínica para inibição do sistema renina-angiotensina (SRA) (por exemplo, hipertensão, proteinúria ou indicação cardíaca) .4{{10}}–42 inibidores da ECA ou BRA podem ser benéficos em pacientes com hipertensão/proteinúria associada ao inibidor do fator de crescimento endotelial vascular (VEGF), embora sejam necessários dados de desfechos específicos para DRC. O uso de inibidor da ECA ou BRA em pacientes com câncer pode estar associado à melhora da sobrevida global.43–48 Uma meta-análise incluindo 11 estudos mostrou benefícios no câncer do trato urinário (razão de risco [HR] 0.22), câncer colorretal (HR 0.22), câncer de pâncreas (HR 0,58) e câncer de próstata (HR 0,14), mas não em câncer de mama ou carcinoma hepatocelular.47 A meta-análise indicou que o uso de inibidores da ECA ou BRA em pacientes com câncer poderia levar a uma redução de 40 por cento no risco de recorrência do câncer e uma redução de 25 por cento no risco de mortalidade. Uma metanálise separada, incluindo 55 estudos, indicou que os inibidores do RAS podem melhorar a sobrevida dos pacientes com câncer, dependendo do tipo de câncer e do tipo de inibidor do RAS.48 O efeito benéfico da inibição do RAS foi demonstrado em neoplasias malignas do trato urinário, como CCR, câncer e câncer de bexiga, bem como câncer gástrico e carcinoma hepatocelular. Mais uma vez, são necessários dados de resultados específicos da DRC.
Os inibidores da ECA ou BRA podem estar associados ao aumento do risco de LRA em pacientes que recebem terapia sistêmica ativa,49,50 e, portanto, as decisões de tratamento devem ser tomadas com uma abordagem individualizada nesses pacientes. Por exemplo, a descontinuação temporária de inibidores da ECA e BRAs pode ser considerada durante o tratamento do câncer.
LRA induzida por contraste.
A LRA induzida por contraste intravenoso é uma questão relevante em pacientes com câncer, especialmente naqueles com comorbidades e/ou TFG reduzida (DRC G3b–G5). Altas doses de meios de contraste e exames repetidos com contraste podem aumentar o risco de LRA. Pacientes ambulatoriais estáveis (pacientes ambulatoriais) têm um risco de LRA menor em comparação com pacientes doentes e instáveis internados com TFG semelhante.51 Em pacientes sem câncer, aqueles com DRC G4-G5 têm uma incidência significativamente maior de LRA induzida por contraste (13,6 por cento vs. 2,7 por cento em pacientes com DRC G3a–G3b), mesmo após hidratação intravenosa profilática.52 Não houve estudos randomizados sobre o risco de administração de radiocontraste em pacientes oncológicos e não há dados suficientes para determinar se pacientes com DRC com câncer devem receber menos meios de contraste tomografia computadorizada (TC). Em uma análise retrospectiva de pacientes com câncer,53 a prevalência de nefropatia induzida por contraste (NIC) foi de 9% com doença renal pré-existente (50% com NIC irreversível) e aproximadamente 5% sem doença renal. Primo et ai. 54 relataram um risco 4.5-mais alto de NIC entre pacientes oncológicos submetidos a TC dentro de 45 dias após a conclusão da quimioterapia em relação àqueles que não receberam quimioterapia ou foram submetidos a TC mais de 45 dias após a conclusão da quimioterapia. No entanto, o conceito de NIC foi questionado com base em resultados de múltiplas análises de escore de propensão, abrangendo mais de 60,000 pacientes, incluindo aqueles com câncer, nos quais o risco de IRA não foi significativamente diferente com contraste versus sem contraste Tomografias computadorizadas. 55,56 Uma revisão sistêmica demonstrou riscos semelhantes de LRA, início de diálise e mortalidade com TC com ou sem contraste.57
Um medo exagerado de nefropatia por radiocontraste pode levar à retenção de estudos diagnósticos benéficos ou intervenções em pacientes com DRC e reduzir o poder diagnóstico dos protocolos de acompanhamento. Portanto, não deve ser negada aos pacientes com DRC uma tomografia computadorizada com meio de contraste se acredita-se que os benefícios superam os riscos da LRA pós-contraste. Na DRC G4-G5, a redução da dose de contraste e o uso de meios de contraste iso-osmolares são preferíveis a não realizar tomografias, embora seu custo-benefício deva ser validado por um estudo controlado.
Atualmente, o uso periprocedimento de solução salina intravenosa e/ou hidratação oral, dependendo do nível de TFG, é frequentemente usado, embora os resultados de estudos prospectivos e metanálises sejam um tanto conflitantes. pacientes com câncer com DRC G3a–G3b, nenhuma profilaxia foi não inferior e econômica em comparação com a hidratação intravenosa na prevenção de LRA pós-contraste.59 Os resultados do estudo PRESERVE de mais de 5.000 pacientes sem câncer não apoiaram a eficácia do sódio bicarbonato e acetilcisteína na prevenção de LRA pós-contraste.60
Um estudo randomizado e controlado de meio de contraste iso-osmolar versus meio de contraste de baixa osmolaridade em pacientes com câncer com DRC G3b–G4, estratificado para pacientes ambulatoriais e internados, é uma prioridade para a pesquisa (Tabela 1). Uma segunda prioridade seria avaliar a hidratação oral versus intravenosa em pacientes com câncer com DRC G3b–G5 (não tratados por diálise) submetidos a repetidas tomografias.
Gerenciando toxicidades renais de tratamentos
Nefrotoxicidade de tratamentos oncológicos. A nefropatia por radiação pode ocorrer após o transplante de células-tronco hematopoiéticas ou após o tratamento com radioisótopos. As drogas anticâncer são uma causa relativamente comum de distúrbios agudos e de DRC, bem como de eletrólitos e ácido-base (Figura 124). As drogas anticâncer podem ser geralmente classificadas como (i) drogas quimioterapêuticas citotóxicas, (ii) agentes de câncer direcionados e (iii) imunoterapias de câncer (Tabela 2). Os quimioterápicos citotóxicos são a causa mais comum de lesão renal e incluem vários agentes, como compostos contendo platina (especialmente cisplatina), ifosfamida, gencitabina, metotrexato e pemetrexed. A lesão tubular aguda (ATI) é a lesão renal mais comum; no entanto, várias outras lesões renais também foram descritas, como microangiopatia trombótica (TMA), podocitopatias, tubulopatias (síndrome de Fanconi, perda de sal e magnésio, diabetes insípido nefrogênico), nefrite tubulointersticial aguda/crônica e nefropatia cristalina.
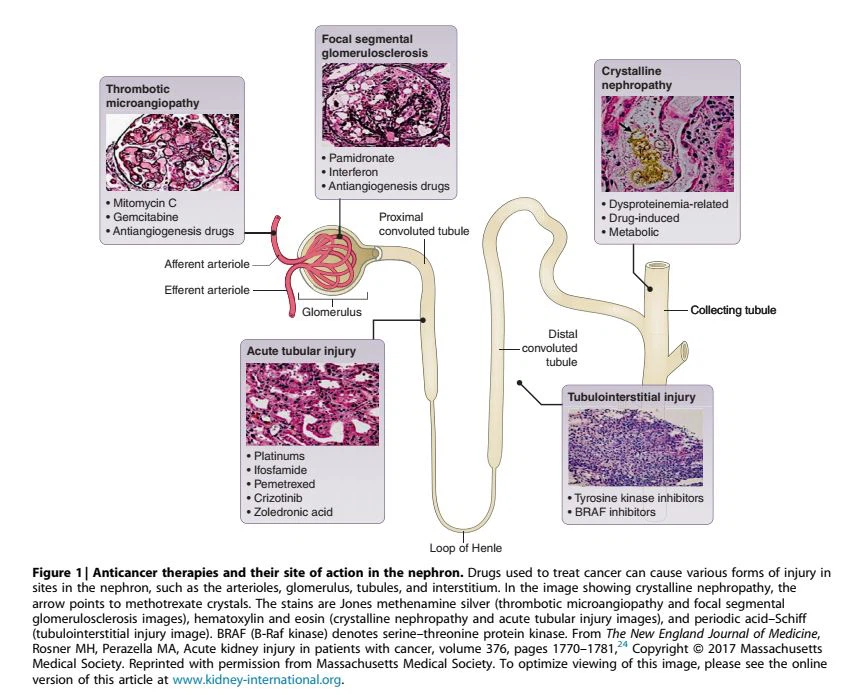
Drogas direcionadas ao câncer tornaram-se cada vez mais importantes para o tratamento de várias doenças malignas, mas os efeitos renais adversos também complicam a terapia. Os medicamentos antiangiogênese estão associados a hipertensão nova ou agravada, proteinúria (às vezes nefrótica) e lesões como MAT, doença de lesão mínima/glomeruloesclerose segmentar focal e nefrite intersticial aguda (NIA). Outros agentes, como o B-Raf e os inibidores da quinase do linfoma anaplásico, causam LRA (ATI e AIN) com menos frequência, enquanto os inibidores de proteassoma podem estar associados à MAT; notavelmente, os inibidores da quinase do linfoma anaplásico ALK (por exemplo, crizotinibe) e os inibidores de CDK4 e CDK6 (por exemplo, abemaciclibe) podem causar um aumento não prejudicial na creatinina sérica devido a um efeito inibitório desses medicamentos na secreção de creatinina, e isso deve ser diferenciado de toxicidade renal genuína.61,62 Os inibidores do fator de crescimento epidérmico, em particular o cetuximab, têm sido associados à hipomagnesemia por perda renal de magnésio.
As imunoterapias contra o câncer também podem causar doença renal. As imunoterapias mais antigas e seus efeitos são bem conhecidos; interferon está associado a diferentes tipos de glomerulonefrite (p. AKI pré-renal e ATI. Os inibidores de checkpoint imunológico são uma terapia relativamente nova e eficaz para um número crescente de cânceres sólidos. Essas drogas foram descritas como causadoras de IRA e proteinúria (às vezes nefrótica); A LRA é devida principalmente à NIA, mas também ocorre ATI. Doença de lesão mínima e doença glomerular relacionada a imunocomplexos também foram descritas com esses medicamentos.
Tanto os mecanismos de nefrotoxicidade dos tratamentos oncológicos quanto as melhores estratégias de manejo para tal toxicidade são amplamente desconhecidos. As abordagens de pesquisa estão descritas na Tabela 1. A nefrotoxicidade deve ser incluída na vigilância de pacientes tratados com imunoterapia e relatada nos registros de medicamentos.
Agentes estimulantes da eritropoietina e terapia com ferro. Atualmente, as indicações de tratamento com agentes estimuladores de eritropoietina (ESAs) e terapia com ferro não são diferentes para pacientes com DRC com ou sem malignidade.63,64 A maioria das diretrizes disponíveis de nefrologia e oncologia sugere o mesmo nível alvo de hemoglobina (1{{9} }–12 g/dl).63–66 As diretrizes KDIGO recomendam um intervalo inferior de 9,0–11,5 g/dl.67 O uso de um intervalo de 9–11,5 g/dl permite a individualização para determinar o melhor perfil de risco-benefício. Para ESA, a dose de nefrologia é sugerida para pacientes com câncer com DRC.68 Dados de meta-análise de 2009 sugeriram que o tratamento com ESAs em pacientes com câncer aumenta a mortalidade e piora a sobrevida geral69; no entanto, uma meta-análise de 91 estudos de 2012 com mais de 20,{25}} participantes não mostrou um impacto direto dos ESAs na progressão da doença do câncer.70 Em um artigo recente, Thavarajah e Choi71 destacaram que, embora as evidências atuais sugiram Os AEEs podem promover progressão ou piorar os resultados em alguns tipos de câncer, não há dados sobre a probabilidade de desenvolvimento de novos cânceres em pacientes em diálise ou naqueles em estágios iniciais de DRC durante a terapia com AEE.
Estudos de registro podem auxiliar em uma melhor compreensão da sobrevida relacionada ao câncer em pacientes com câncer tratados com ESAs. Avaliar novos tratamentos de anemia que estimulam a produção endógena de eritropoietina e aumentam a disponibilidade de ferro, como inibidores de prolil hidroxilase do fator induzível por hipóxia,22 em pacientes com câncer com DRC também será importante.
Ajustes de tempo e dosagem de drogas anticâncer em pacientes com DRC G3-G5D.
As evidências disponíveis sugerem que não ajustar as doses de drogas anticancerígenas em pacientes com DRC é deletério. Em um estudo prospectivo de 143 pacientes com câncer colorretal que receberam doses padrão de capecitabina e oxaliplatina, entre os 50 pacientes com depuração de creatinina<60 ml/min,="" cytopenia="" and="" diarrhea="" were="" significantly="" higher="" relative="" to="" patients="" with="" creatinine="" clearance="" of="" $ 60="" ml/min,="" and="" effificacy="" of="" the="" drugs="" was="" reduced.72 alternatively,="" in="" a="" prospective="" study="" of="" more="" than="" 600="" breast="" cancer patients,="" adjusting="" the="" dosage="" of="" anticancer="" drugs="" in="" patients with="" creatinine=""><60 ml/min="" when="" necessary="" resulted="" in="" comparable="" toxicity="" and="" effectiveness="" relative="" to="" standard="" dosing="" in="" patients="" with="" creatinine="" clearance="" of="" $60="" ml/ min.73 in="" hemodialysis="" patients,="" active="" catabolites="" of="" certain drugs="" have="" the="" potential="" to="" accumulate="" and="" lead="" to="" unexpected="" adverse="" events,74–76 and="" dose="" adjustment="" is="" crucial="" to avoid="" accumulation="" and="" toxicity.="" published="" clinical="" recommendations="" regarding="" optimal="" timing="" and="" dose="" adjustment="" of anticancer="" drugs="" (also="" in="" timing="" related="" to="" the="" start="" of="" the dialysis="" session)="" in="" ckd="" g5d="" cancer="" patients="" do="" exist77,78; however,="" the="" recommendations="" were="" derived="" based="" on="" case reports="" or="" small="" case="" series.="" in="" addition,="" a="" nationwide="" study in="" japan="" has="" indicated="" there="" is="" a="" gap="" between="" recommendations="" and="" clinical="" practice="" in="" dose="" adjustment="" of="" anticancer agents="" in="" ckd="" g5d="">
Não há dados disponíveis sobre pacientes com DRC avançada e diálise peritoneal e, portanto, estudos farmacocinéticos e farmacodinâmicos são necessários.
Tomada de decisão para iniciar ou encerrar a terapia de substituição renal em pacientes com câncer de órgãos sólidos.
Atualmente, existem variações específicas de cada país nas abordagens para iniciar ou suspender a diálise em pacientes com cânceres de órgãos sólidos (ou hematológicos). Embora existam sistemas de pontuação para prever a sobrevida de pacientes em diálise, eles podem e devem ser aprimorados incluindo a presença de câncer ativo e/ou seu prognóstico. A retirada da diálise crônica leva à morte em poucas semanas; portanto, quando o prognóstico de sobrevida relacionado ao câncer é inferior a 2 semanas, a diálise deve ser interrompida. A solicitação ativa de diretivas antecipadas de vontade por meio do trabalho em equipe interdisciplinar pode ajudar médicos e pacientes a evitar decisões difíceis em situações de emergência. Determinar as preferências dos pacientes em relação à diálise de longo prazo, diálise experimental por tempo limitado, tratamento conservador da DRC ou cuidados paliativos é fundamental.

MANEJO E TRATAMENTO DO CÂNCER RENAL
Epidemiologia, prevalência e tipo de carcinoma de células renais
The World Health Organization has estimated that the age-standardized incidence of kidney cancer worldwide was 4.5 per 100,000 persons in 2018.80 RCC, which refers to cancer that originated from renal epithelium, accounts for >90 por cento dos cânceres no rim.81 A incidência de CCR predomina em homens (1,5:1,0, homens para mulheres) e tem um pico de incidência em pessoas com idade entre 60 e 70 anos.81 A incidência de CCR varia amplamente globalmente, mas está aumentando em muitos países.82 O aumento da incidência está relacionado principalmente a mudanças na detecção do tumor e nas práticas diagnósticas (disseminação da TC/ultrassom), levando ao aumento dos diagnósticos de CCR em estágio inicial. Fatores de risco estabelecidos são tabagismo, obesidade, hipertensão, DRC, diabetes e certos fatores genéticos.82 Não está claro se atividade física, dieta, consumo de álcool e exposições ambientais aumentam o risco de CCR.
Apesar das recentes melhorias em seu tratamento, o CCR, quando metastático, continua sendo uma doença letal. As taxas de mortalidade por CCR variam de acordo com a extensão das instalações e tratamentos urológico-oncológicos disponíveis.83 Na maioria dos países desenvolvidos, as taxas de mortalidade por CCR são estáveis ou estão diminuindo como resultado de esforços de triagem, diagnóstico precoce e melhores tratamentos e sua disponibilidade.82
As síndromes hereditárias de CCR são responsáveis por 2% a 3% de todos os casos de CCR,84 e muitas variantes genéticas têm sido associadas a CCR.84,85 A causa hereditária mais comum de CCR é a síndrome de von Hippel-Lindau, na qual há uma vida inteira incidência cumulativa de CCR de aproximadamente 70 por cento.84 As formas esporádicas geralmente estão associadas a alterações estruturais do braço curto do cromossomo 3.
Função renal no CCR
A função renal prejudicada é comum em pacientes com CCR, seja como uma condição pré-existente ou como consequência do câncer e sua terapia.86 CCR e função renal prejudicada compartilham fatores de risco renais intrínsecos e comorbidades sistêmicas (Figura 2). 87,88 Os fatores de risco relacionados ao câncer para função renal prejudicada no CCR incluem: infiltração maligna, que pode envolver parênquima renal e/ou veia renal e veia cava inferior; síndromes paraneoplásicas causadas por doença de citocinas ou doença imunogênica, incluindo nefropatias paraneoplásicas ou hipercalcemia por produção de proteína semelhante ao paratormônio89; e obstrução do trato urinário.

A ressecção cirúrgica continua sendo a modalidade de tratamento preferencial na maioria dos casos de CCR. Infelizmente, a nefrectomia foi reconhecida como um fator de risco independente para lesão renal (Figura 3).86,90 Após a nefrectomia, a redução da massa renal é seguida por uma diminuição da função renal, especialmente em pacientes com doenca renal; além disso, os glomérulos remanescentes podem sofrer lesões de hiperfiltração.87,91

Sabe-se que pacientes com DRC apresentam risco aumentado de CCR.92,93 Embora a causa do câncer renal na DRC seja desconhecida, vários fatores relacionados à lesão renal têm sido propostos para explicar essa relação,94 incluindo fibrose renal e atrofia tubular, como bem como inflamação crônica relacionada à uremia, estresse oxidativo, função imunológica comprometida, processo de diálise, medicamentos e doenças comórbidas.86 O risco de CCR aumenta com o aumento da gravidade da doença renal.92 A associação observada entre DRC e o risco futuro de CCR não é necessariamente causador; indivíduos com função renal comprometida são submetidos a vigilância médica mais intensiva em relação à população em geral, e isso pode levar ao aumento da detecção incidental de tumores renais indolentes localizados por meio de imagens abdominais.
A DRC é fator prognóstico para CCR e aumenta os riscos de mortalidade,95 eventos cardiovasculares, insuficiência renal e hospitalização prolongada.10 A piora da função renal pode impedir ou retardar a terapia antineoplásica. Além disso, a dosagem do medicamento pode ser inadequada em pacientes em diálise, que apresentam aumento da depuração de certos medicamentos.
Tipo de cirurgia e resultados renais
Current guidelines recommend partial nephrectomy for the resection of tumors stage T1 (i.e., tumors #7 cm, confined to the kidney) to preserve as much normal renal parenchyma as possible.96,97 The technique can also be considered for tumors staged T2 (i.e., tumors >7 cm, confinado ao rim) e T3a (ou seja, tumores que se estendem macroscopicamente para a veia renal, afetando seus ramos ou invadindo a gordura perinéfrica ou do seio renal). A nefrectomia citorredutora não deve ser realizada em pacientes classificados como de baixo risco com base na classificação do Memorial Sloan Kettering Cancer Center.98 Embora criticados pela metodologia, os estudos randomizados CARMENA e SURTIME recentemente relatados apoiam a oferta de terapia sistêmica antes da nefrectomia citorredutora para CCR metastático.99,100 Confiável os critérios para selecionar pacientes para inibidores neoadjuvantes de tirosina quinase (TKIs) com nefrectomia citorredutora permanecem em grande parte indefinidos. No entanto, os resultados dos estudos acima mencionados indicam que pacientes com características de risco devem receber terapia sistêmica, e não nefrectomia citorredutora, como o manejo inicial da doença. Também é importante ressaltar que a cirurgia ainda é uma ferramenta valiosa no manejo do CCR metastático. Portanto, pacientes de risco intermediário com metástases potencialmente ressecáveis podem ser considerados para nefrectomia citorredutora e metastasectomia sem terapia sistêmica como tratamento inicial da doença. Atualmente, não há dados sobre o uso de inibidores de checkpoint antes da nefrectomia citorredutora.
Preocupações relacionadas aos riscos perioperatórios e acompanhamento pós-operatório
A prevenção da DRC G5 após a cirurgia envolve identificar e reduzir os riscos de LRA e tratar suas complicações.91 Os pacientes em risco de LRA incluem aqueles com DRC, diabetes mellitus, hipertensão, proteinúria, idade avançada ou tecido não neoplásico anormal próximo ao tumor, bem como pacientes que fumam.91 Bhindi et al.101 recentemente desenvolveram modelos para predizer os resultados da função renal após nefrectomia parcial e radical com base nessas e em outras características pré-operatórias; no entanto, as fórmulas precisam ser validadas e confirmadas para generalização. Ter medidas de TFG mais precisas, melhores imagens e melhor identificação de grupos de risco ajudariam nos processos relacionados à previsão.
Intraoperative steps for preventing kidney injury include minimizing nephron loss and devascularization, avoiding irreversible ischemic damage, and maintaining adequate renal perfusion during surgery. A variety of pharmacologic manipulations (mannitol, dopamine, fenoldopam, antioxidants, growth factors, porphyrins, mitochondria-protecting amino acids) have been used in an effort to abrogate the negative effects of ischemia, although results of most translational studies to date have been negative. Intraoperative maneuvers for preventing irreversible ischemic injury include the use of hypothermia, early unclamping, and zero ischemia. Results of a systematic review102 indicate there is no evidence to suggest that limited ischemia time (#25 min) has a higher risk of reduced kidney function after partial nephrectomy compared with a zero ischemia technique. Prolonged warm ischemia (>25-30 min) pode causar um insulto isquêmico irreversível ao rim tratado cirurgicamente.
O manejo geral pós-operatório inclui acompanhamento adequado com reconhecimento precoce e intervenção oportuna, encaminhamento precoce à nefrologia de pacientes de alto risco, evitar complicações pós-cirúrgicas, evitar nefrotoxinas e hipoperfusão renal e corrigir fatores reversíveis relacionados à LRA. As estratégias para prevenir a progressão da DRC para insuficiência renal incluem o monitoramento regular da função renal, medindo a creatinina sérica e a TFGe, bem como intervenções imediatas para limitar o início ou a progressão da doença renal, incluindo o controle da hipertensão e do diabetes mellitus, evitando nefrotoxinas e outros fatores agravantes , e corrigir anemia, desnutrição e acidose metabólica. O monitoramento repetido a longo prazo da eGFR é indicado em casos de função renal prejudicada antes ou após a cirurgia.
Novas terapias direcionadas e efeitos colaterais renais
Os agentes de direcionamento para o tratamento de RCC metastático incluem tratamentos com receptor de fator de crescimento endotelial antivascular/fator de crescimento endotelial vascular, inibidores de alvo de mamífero de rapamicina e inibidores de checkpoint imunológico. Estes são usados como monoterapias e terapias combinadas. A nefrotoxicidade relacionada a drogas anticâncer é uma causa comum e notável de lesão renal, potencialmente causando hipertensão, proteinúria, IRA e distúrbios eletrolíticos.91 As etiologias incluem necrose tubular aguda ou lesão e uma variedade de lesões glomerulares e vasculares.
Inibidores da tirosina quinase.
Em pacientes em diálise, o tratamento com TKIs é seguro e eficaz.103–111 Estudos retrospectivos indicam que o uso de TKIs multidirecionados (sorafenibe, sunitinibe, pazopanibe, axitinibe, cabozantinibe e lenvatinibe) pode prolongar a expectativa de vida no contexto de doença renal metastática clara carcinoma celular, mesmo em pacientes em diálise.107
Os pacientes em diálise que recebem TKIs não precisam de um número maior de sessões de diálise. A maioria dos eventos adversos com TKIs em pacientes em diálise é de gravidade leve, sendo a anemia o evento adverso mais comum relatado.103 O monitoramento do uso de heparina em pacientes em diálise submetidos ao tratamento com TKI pode ajudar a mitigar o risco de sangramento. Para pacientes não submetidos à diálise, mas com DRC G3a–G5, a idade e as comorbidades estão associadas ao aumento da pressão arterial.23 A normalização da pressão arterial na linha de base e o monitoramento durante o tratamento são de suma importância,112 embora o controle da pressão arterial possa ser mais desafiador do que em pacientes com melhor função renal.113 Como ponto prático, para pacientes com doença renal, incluindo aqueles em diálise, os TKIs podem ser iniciados com uma dose menor que a padrão e titulados com base na tolerabilidade. Devido ao grande volume de distribuição de TKIs, a superhidratação deve ser evitada com o uso de TKIs.
Inibidores de checkpoint imunológico.Embora rara, nefrite autoimune foi relatada em pacientes tratados com inibidores de checkpoint imunológico.23 Toxicidade renal grave (nota $3) é encontrada em aproximadamente 1% dos pacientes e geralmente é revertida com a descontinuação do agente responsável e terapia com esteróides.114 Os inibidores de checkpoint podem ser reiniciado quando a dosagem de prednisona for #10 mg (embora esta recomendação não seja apoiada por nenhum estudo prospectivo). As opções não esteroidais incluem micofenolato de mofetil e rituximabe e são indicadas em raros casos refratários a esteroides. Em casos selecionados de lesão renal, uma biópsia renal pode ser considerada.
Dados sobre inibidores de checkpoint em pacientes com doença renal ou em diálise são extremamente limitados, geralmente a relatos de casos ou séries de casos. Atualmente, não há evidências para apoiar a redução do número de tratamentos com inibidores de checkpoint em pacientes com TFG reduzida ou em diálise.
CONCLUSÕES
Os participantes da conferência enfatizaram a importância da colaboração entre especialistas em nefrologia e hematologia/oncologia no atendimento clínico, bem como em ensaios clínicos.115 Questões importantes relacionadas ao gênero em onco-nefrologia que não foram investigadas incluem a epidemiologia do câncer em pacientes com DRC e insuficiência renal em pacientes com câncer, bem como a resposta ao tratamento do câncer no cenário de DRC. As limitações dos métodos atuais para estimar a TFG e determinar a função renal têm implicações clínicas negativas, e espera-se que novas abordagens para medir a função renal estejam disponíveis em um futuro próximo. No entanto, os pacientes hematológicos/oncológicos devem ser submetidos a avaliações da função renal, incluindo estimativa da TFG e determinação do grau de proteinúria. No cenário de malignidade de órgãos sólidos, investigações renais importantes incluem avaliação da função renal, bem como comorbidades, equilíbrio ácido-base, eletrólitos e análise de urina. Em pacientes com DRC, a melhor abordagem atual para dosagem de agentes quimioterápicos é usar a equação CKD-EPI. Estudos pós-comercialização que incluam pacientes com DRC poderiam informar a dosagem de medicamentos oncológicos em pacientes com DRC G3b–G5D, uma área com grande carência de dados. Ensaios especificamente focados em pacientes com CCR com função renal comprometida são uma área de necessidade urgente.
De: 'Compreendendo a insuficiência renal e malignidades de órgãos sólidos, e gerenciando o câncer de rim' porCamilo Porta, et al.
---Internacional do Rim (2020) 98, 1108–1119
