Diferenças sexuais na obesidade, metabolismo lipídico e inflamação: um papel para os cromossomos sexuais?
Mar 24, 2022
Contato: Audrey Hu Whatsapp/hp: 0086 13880143964 E-mail:audrey.hu@wecistanche.com
Temeka Zore, Maria Palafox, Karen Reue
ABSTRATO
Fundo: Sexodiferenças na obesidade e doenças relacionadas estão bem estabelecidas. Os hormônios gonadais são um dos principais determinantes dessessexodiferenças. No entanto, as diferenças sexuais no tamanho e composição do corpo são evidentes antes da exposição aos hormônios gonadais, fornecendo evidências de contribuições gonadais independentes atribuíveis ao complemento cromossômico sexual XX ou XY. Estudos genéticos em larga escala revelaram diferenças entre homens e mulheres na arquitetura genética da quantidade de tecido adiposo e na distribuição anatômica. No entanto, esses estudos normalmente negligenciaram os cromossomos X e Y.
Escopo da revisão: Aqui discutimos como osexocomplemento cromossômico pode influenciar a obesidade, os níveis lipídicos e a inflamação. Anomalias dos cromossomos sexuais humanos, como a síndrome de Klinefelter (XXY), bem como modelos de camundongos com alterações projetadas emsexocomplemento cromossômico, suportam um papel importante para os cromossomos sexuais na obesidade e no metabolismo. Em particular, o modelo de camundongo Four Core Genotypes, consistindo em camundongos XX com ovários ou testículos, e camundongos XY com ovário ou testados revelou um efeito da dosagem do cromossomo X na adiposidade, hiperlipidemia e inflamação, independentemente das gônadas masculinas ou femininas. . Os mecanismos podem incluir expressão aumentada de genes que escapam da inativação do cromossomo X.
Principais conclusões: Embora menos estudados do que os efeitos dos hormônios gonadais,sexoos cromossomos exercem efeitos independentes e interativos sobre a adiposidade, metabolismo lipídico e inflamação. Em particular, a presença de dois cromossomos X tem sido associada ao aumento da adiposidade e dislipidemia em modelos de camundongos e em homens XXY. A expressão aumentada de genes que escapam da inativação do cromossomo X pode contribuir, mas é necessário mais trabalho.
Palavras-chaveGenética; Hormônios gonadais; Tecido adiposo;Sexoanomalias cromossômicas; inativação do cromossomo X; Modelos de mouse
para que serve o cistanche: melhorar a sexualidade
1. DIMORFISMO SEXUAL NA DOENÇA
O estudo desexoas diferenças na fisiologia ganharam força no que se refere à compreensão das diferenças homem/mulher na suscetibilidade à doença. As mulheres sofrem mais frequentemente de doenças autoimunes (por exemplo, lúpus eritematoso sistêmico, esclerodermia, síndrome de Sjögren), bem como osteoporose, doença de Alzheimer e depressão clínica [1e6]. O autismo ocorre em taxas mais altas em meninos do que em meninas, e as diferenças entre os sexos também são observadas em doenças neurológicas, como a doença de Parkinson e a esquizofrenia, para citar algumas [7e9]. Na doença cardiovascular e acidente vascular cerebral, existem diferenças entre os sexos na idade de início, patologia da doença e mortalidade [10].
Algumsexodiferenças nas doenças humanas estão diretamente relacionadassexocomplemento cromossômico em mulheres (XX) e homens (XY). Os homens são mais comumente afetados por doenças ligadas ao X, como daltonismo, distrofia muscular de Duchenne e hemofilia. As mulheres podem ser protegidas (ou experimentar gravidade atenuada) desses distúrbios recessivos porque possuem dois cromossomos X [11]. A inativação aleatória de um cromossomo X em células femininas durante o desenvolvimento inicial silencia o cromossomo X que carrega um gene mutante em aproximadamente metade das células femininas, permitindo a expressão exclusiva de um gene selvagem nessas células. Um exemplo extremo da influência do genótipo XX versus XY na gravidade da doença na síndrome de Rett, que resulta de uma mutação no gene MECP2 no cromossomo X. As mulheres afetadas por mutações de Rett experimentam deficiências progressivas do desenvolvimento neurológico, levando a deficiências na aprendizagem, comunicação, coordenação e outras funções cerebrais. Por outro lado, homens com mutações MECP2 geralmente morrem no útero ou na infância [12].
Aqui vamos discutir como asexocomplemento cromossômico pode influenciar fatores subjacentes a distúrbios metabólicos, como obesidade, dislipidemia e inflamação. É bem conhecido que os hormônios gonadais têm fortes efeitos no armazenamento de gordura e suscetibilidade a doenças relacionadas, como doenças cardiovasculares e diabetes tipo 2 [13]. Uma vez que as gônadas femininas são normalmente encontradas junto com os cromossomos XX e as gônadas masculinas com os cromossomos XY, os papéis independentes dos hormônios gonadais esexocromossomos não foram apreciados. No entanto, anomalias dos cromossomos sexuais humanos, como a síndrome de Klinefelter (XXY) e a síndrome de Turner (XO), bem como modelos de camundongos com alterações projetadas no complemento dos cromossomos sexuais, suportam um papel importante para os cromossomos sexuais na obesidade e no metabolismo.
2. DIFERENÇAS SEXUAIS NA ADIPOSIDADE E OBESIDADE HUMANA
O tecido adiposo serve como um eficiente depósito de armazenamento de energia. Também tem papéis ativos na captação de ácidos graxos das lipoproteínas circulantes produzidas em resposta a uma refeição e na liberação regulada de ácidos graxos para uso por outros tecidos entre as refeições ou durante a atividade física. Existem diferenças importantes entre homens e mulheres na distribuição do tecido adiposo, com os homens acumulando maiores quantidades de tecido adiposo visceral e as mulheres geralmente com maior acúmulo de gordura nos depósitos subcutâneos (glúteo femoral) [14,15]. A distribuição de gordura específica do sexo é influenciada por vários fatores, incluindo dieta e estado hormonal [16]. Um colaborador desexoO viés na distribuição do tecido adiposo pode ser a taxa de captação direta de ácidos graxos pelos tecidos, um processo que ocorre independentemente da lipoproteína lipase (a enzima responsável pela liberação de ácidos graxos das lipoproteínas). A captação direta de ácidos graxos é maior no depósito femoral glúteo em mulheres e no depósito abdominal em homens [17].
Tanto a massa gorda global quanto o acúmulo de gordura visceral estão fortemente associados ao desenvolvimento de doenças cardiovasculares, acidente vascular cerebral, hipertensão e resistência à insulina [15,18,19]. As medidas padrão para o acúmulo de gordura em humanos incluem o índice de massa corporal (peso em função da altura), que reflete a adiposidade de todo o corpo e a relação cintura-quadril, que fornece uma indicação da distribuição de gordura, com a medida da cintura como proxy. para gordura visceral e a medida do quadril para gordura glútea [19]. Estudos seminais realizados na década de 1980 forneceram evidências de que a adiposidade geral, bem como a massa de gordura subcutânea, têm uma herdabilidade de aproximadamente 30% [20]. Essa estimativa foi corroborada por um estudo de 1990 em gêmeos caucasianos do sexo masculino que mostrou uma herdabilidade de 31% da relação cintura-quadril, enquanto um estudo populacional mais recente estimou a herdabilidade da mesma característica em 39% [21,22]. Algumas estimativas indicam que a hereditariedade da distribuição de gordura é maior nas mulheres do que nos homens [19]. A distribuição de gordura e a hereditariedade também diferem entre os grupos étnicos [23,24]. Uma abordagem para identificar os genes que contribuem para asexodiferenças no acúmulo e distribuição de tecido adiposo são estudos de associação genômica ampla (GWAS) em grandes coortes humanas. Essa abordagem tipifica variantes genéticas em todo o genoma e correlaciona sua ocorrência com uma característica para identificar loci que estão associados. GWAS realizado em centenas de milhares de pessoas identificaram mais de 100 loci genéticos que abrigam variantes genéticas comuns que influenciam a adiposidade [25e27]. É importante ressaltar que pelo menos 17 loci que estão associados ao índice de massa corporal também foram identificados na GWAS para diabetes tipo 2 [25].
A análise dos dados acumulados do GWAS revelou uma arquitetura genética distinta para loci que afetam a adiposidade em machos e fêmeas. Por exemplo, uma meta-análise de mais de 50 estudos GWAS com relação cintura-quadril (ajustada para gordura total) em mais de 200,000 indivíduos identificaram 49 loci, 20 dos quais mostraramsexoefeitos específicos, com 19 deles tendo efeitos mais fortes em mulheres [28]. Esses loci representam um rico recurso para a identificação de fatores genéticos de viés de sexo para composição corporal e distribuição de gordura, embora, atualmente, esses loci juntos representem apenas uma pequena porcentagem da variação genética na adiposidade. Ainda há muito trabalho a ser feito, incluindo a identificação das variantes causais em cada locus e seu mecanismo de ação para influenciar a adiposidade. É importante notar que essas análises não levaram em conta loci nos cromossomos X ou Y, deixando uma lacuna em nosso conhecimento sobre como as variações genéticas em X e Y podem contribuir parasexodiferenças na adiposidade. As seções a seguir descrevem estudos fora do GWAS que informaram sobre o papel dos cromossomos X e Y na adiposidade e doenças metabólicas.

extrato de cistanche tubolosa
3. DIFERENÇAS SEXUAIS NA EXPANSÃO DO TECIDO ADIPOSO
Tem sido sugerido que os adipócitos em depósitos femorais glúteos (e outros depósitos subcutâneos) conferem melhor saúde metabólica devido à capacidade de expandir para armazenar mais gordura recrutando novos adipócitos [16,29,30]. Anteriormente, pensava-se que os camundongos machos exibiam maior expansão da massa gorda induzida pela dieta (em depósitos viscerais e subcutâneos) do que as fêmeas, e isso se deve em parte aos efeitos dasexohormônios [31e33]. No entanto, um estudo recente demonstra que em camundongos C57BL/6J, osexoas diferenças no ganho de peso induzido pela dieta dependem fortemente da idade dos camundongos quando alimentados com uma dieta rica em gordura. Em camundongos juvenis (com 6 semanas de idade), alimentar uma dieta rica em gordura por 3 meses levou a um maior ganho de peso percentual nos machos do que nas fêmeas. No entanto, em camundongos adultos (com 31 semanas de idade), a tendência foi revertida e as fêmeas ganharam um percentual de peso corporal substancialmente maior em resposta à dieta rica em gordura [34].
Um potencial contribuinte parasexodiferenças na expansão do tecido adiposo é o número de células precursoras de adipócitos (células-tronco pluripotentes que podem se diferenciar em adipócitos, condrócitos ou osteoblastos) em depósitos de gordura gonadal ou subcutânea de camundongos. Em uma dieta com baixo teor de gordura, camundongos C57BL/6J fêmeas têm mais células precursoras de adipócitos do que machos nas bolsas de gordura gonadal (visceral) e inguinal (subcutânea) [35e 37]. Quando alimentados com uma dieta rica em gordura (45 por cento calorias como gordura), camundongos fêmeas apresentaram aumento de células precursoras de adipócitos e adipócitos maduros na gordura gonadal, mas os machos não aumentaram as células adiposas maduras na gordura gonadal [36]. Outros estudos, que empregaram marcação de pulso ou rastreamento de linhagem para seguir o destino das células progenitoras de adipócitos em proliferação, inferiram que a gordura gonadal masculina exibe hiperplasia em resposta a uma dieta rica em gordura, enquanto as mulheres exibem hiperplasia de adipócitos em depósitos de gordura gonadal e subcutânea. 38,39]. osexo-padrões específicos foram revertidos por ovariectomia em camundongos fêmeas ou administração de estrogênio em camundongos machos, sugerindo um papel dos hormônios gonadais [37]. Esses estudos provaram ser valiosos, mas estudos adicionais de recrutamento e renovação de adipócitos em depósitos de gordura de ambos os sexos são necessários para esclarecer discrepâncias entre estudos que usaram metodologias distintas e fornecer detalhes adicionais.
4. INFLUÊNCIAS GONADAIS E CROMOSSÔMICAS NA ADIPOSIDADE
Os hormônios gonadais têm efeitos importantes no armazenamento de gordura e doenças relacionadas, como evidenciado por comparações de mulheres na pré-menopausa e pós-menopausa. Após a menopausa e redução nos níveis de estrogênio e outros hormônios gonadais, as mulheres geralmente experimentam aumento do armazenamento de gordura nos depósitos abdominais e aumento da ocorrência de doenças cardiovasculares, hiperlipidemia, resistência à insulina e hipertensão [14,40e43]. No entanto, a redução de curto prazo nos níveis de estrogênio (4 semanas) não levou a um armazenamento de gordura alterado, embora tenha afetado os níveis de triglicerídeos circulantes pós-prandiais [44]. Por outro lado, a supressão de curto prazo (4 semanas) dos níveis de testosterona em homens levou ao aumento do armazenamento de ácidos graxos derivados de refeições no depósito de gordura femoral glútea [45]. Os efeitos dos hormônios gonadais no desenvolvimento e metabolismo do depósito de gordura são provavelmente influenciados por inúmeras variáveis, incluindo níveis hormonais e níveis de receptores de estrogênio e andrógeno [46].
Além dos papéis bem estabelecidos dos hormônios gonadais, evidências acumuladas apoiam um papel fundamental para osexocromossomos na determinação de diferenças sexuais na adiposidade. A presença de cromossomos XX em mulheres e cromossomos XY em homens determina o desenvolvimento de ovários ou testículos, respectivamente [47]. Especificamente, o gene SRY (sex-determining region Y) presente no cromossomo Y codifica um fator de transcrição que inicia o desenvolvimento testicular em embriões XY e a subsequente elaboração de hormônios testiculares. A falta de um gene SRY em um embrião (devido a cromossomos XX ou deleção do gene SRY) leva ao desenvolvimento de ovários e à produção de hormônios ovarianos.Sexodiferenças na composição corporal são evidentes antes da exposição aos hormônios gonadais. Por exemplo, durante o desenvolvimento embrionário humano e de camundongos, os fetos masculinos mostram um tamanho maior do que os fetos femininos, mesmo antes da diferenciação gonadal [48,49]. As crianças continuam a exibir diferenças sexuais no peso corporal ao nascer, com bebês do sexo masculino geralmente pesando mais do que bebês do sexo feminino, em parte devido ao maior comprimento do corpo e maior circunferência da cabeça [50]. As diferenças entre homens e mulheres em altura, peso, massa magra e massa de gordura corporal total persistem na infância, antes da puberdade [51].
Uma abordagem para estudar os efeitos dasexocomplemento cromossômico é avaliar a adiposidade e características relacionadas em indivíduos com síndrome de Klinefelter (XXY) ou síndrome de Turner (XO). A síndrome de Klinefelter é a mais comumsexodistúrbio cromossômico, ocorrendo em aproximadamente 1 em 660 nascimentos, e é uma causa frequente de infertilidade e hipogonadismo em homens [52]. Esses homens geralmente apresentam hábito corporal eunucoide, testículos pequenos, hipogonadismo hipogonadotrófico e infertilidade [53]. Indivíduos com Klinefelter demonstraram ter uma incidência quase cinco vezes maior de desenvolver síndrome metabólica [54], definida como a ocorrência de pelo menos três dos seguintes: obesidade abdominal, níveis elevados de glicose em jejum, níveis elevados de triglicerídeos, níveis reduzidos de níveis de lipoproteína de densidade e hipertensão [55]. Homens XXY também têm um risco aumentado de resistência à insulina e diabetes tipo 2 [56,57]. É possível que o aumento do risco de síndrome metabólica e resistência à insulina em indivíduos XXY seja secundário ao aumento da obesidade abdominal, que, por sua vez, pode resultar de hipogonadismo e baixos níveis de testosterona em homens XXY [54,56,58]. É importante ressaltar que estudos de meninos XXY pré-púberes (idade média < 11)="" identificaram="" aumento="" da="" massa="" de="" gordura="" corporal="" e/ou="" circunferência="" da="" cintura="" antes="" da="" influência="" de="" níveis="" alterados="" de="" hormônios="" gonadais="" na="" puberdade="" [59,60].="" isso="" sugere="" que="" o="" próprio="" complemento="" do="" cromossomo="" sexual="" xxy="" pode="" afetar="" a="" adiposidade="" e="" características="" metabólicas="">
A síndrome de Turner (ST) é a anomalia cromossômica sexual mais comum que afeta as mulheres, com incidência de 1 em 2.500 e 3.000 nascidos vivos (8). As mulheres com ST são caracterizadas por baixa estatura, pescoço alado e infantilismo sexual com disgenesia gonadal [61,62]. As mulheres com ST também têm defeitos cardíacos congênitos, o que pode predispor a doenças cardíacas que se desenvolvem independentemente de fatores metabólicos [63]. Relevante para a doença metabólica, as mulheres XO reduziram drasticamente os níveis de hormônios gonadais [64]. Uma vez que os estrogênios e progestinas em mulheres normais na pré-menopausa conferem proteção contra a obesidade abdominal e resistência à insulina e promovem o armazenamento de gordura nos coxins adiposos femorais glúteos [40], os baixos níveis desses hormônios podem obscurecer quaisquer efeitos diretos do complemento cromossômico XO no metabolismo. Consistente com baixos níveis de hormônios gonadais, as mulheres TS têm um aumento de quatro vezes no risco de diabetes tipo 2 e um aumento de três vezes na mortalidade geral [65]. Um papel potencial para a programação fetal precoce foi proposto para contribuir para as anormalidades metabólicas em mulheres com ST, o que é consistente com baixo peso ao nascer e alto peso corporal na vida adulta [66]. Outros dados mostram um papel para o número de cromossomos sexuais, conforme descrito abaixo.
O efeito de confusão dos níveis aberrantes de hormônios gonadais em mulheres XO torna difícil chegar a conclusões sobre a influência do complemento cromossômico sexual na homeostase metabólica desses indivíduos. De uma perspectiva experimental, seria valioso comparar os efeitos de um único cromossomo X em mulheres TS com indivíduos com dois cromossomos X em um fundo de hormônios gonadais igualmente baixos. A última condição é aproximada em mulheres XX com insuficiência ovariana primária (IOP) e níveis baixos de hormônios gonadais correspondentes. Uma comparação dos perfis lipídicos em mulheres com ST e POI (combinação de idade e massa corporal) duas semanas após a interrupção da terapia de reposição de estrogênio mostrou que as mulheres com ST tinham um perfil lipídico mais aterogênico [67]. Como as mulheres TS e POI reduziram as contribuições de hormônios gonadais em comparação com as mulheres normais e foram pareadas quanto ao estilo de vida e composição corporal, os pesquisadores levantaram a hipótese de que alguns efeitos metabólicos em mulheres TS podem ser atribuídos à dosagem alterada do cromossomo X [57,67]. É importante reconhecer, no entanto, que as comparações entre mulheres TS e POI permanecem confusas pelo fato de que indivíduos TS têm desenvolvimento aberrante e secreção de hormônio ovariano prejudicada durante toda a vida, enquanto mulheres POI são normais durante o desenvolvimento e só são afetadas mais tarde na vida. .
Anomalias adicionais dos cromossomos sexuais que ocorrem em humanos incluem a síndrome de Swyer e a síndrome do Triplo X. A síndrome de Swyer, também conhecida como disgenesia gonadal XY, é um distúrbio raro do desenvolvimento sexual em que indivíduos 46, XY apresentam comprometimento do desenvolvimento do tecido gonadal [68]. Esses indivíduos apresentam-se externamente como mulheres, mas não desenvolvem ovários funcionais e não passam pela puberdade, a menos que sejam tratados com terapia hormonal. Essa condição pode ser devido a mutações no gene SRY (que se acredita estar na base de 10 a 20% dos casos) ou mutações em outros genes [68]. A síndrome do Triplo X (47, XXX) é caracterizada pela apresentação variável de fenótipos como alta estatura, distúrbios cognitivos e comportamentais e problemas dentários [69]. No momento, nenhum estudo foi relatado com tamanhos de amostra adequados de síndromes de Swyer ou XXX para analisar os efeitos dessas condições na adiposidade ou características metabólicas relacionadas. Deve-se notar que nas células XO, XX e XXX, a inativação do cromossomo X silencia a maioria dos genes em todos, exceto em um único cromossomo X. A ocorrência de anormalidades nas síndromes de Turner (XO) e XXX, portanto, apoia a visão de que a dosagem do cromossomo X é importante, apesar do processo de inativação de todos, exceto um X. Possíveis razões para a importância de ter exatamente dois cromossomos X é discutido nas seções 5 e 8.

benefício do extrato de cistanche tubolosa: tratamento de doenças renais
5. UM PAPEL PARA XX DOSAGEM DE CROMOSSOMOS EM DIFERENÇAS SEXUAIS NA ADIPOSIDADE
Estudos conclusivos de alterações metabólicas em homens XXY e mulheres XO foram dificultados pela falta de grupos de controle adequados com níveis semelhantes de hormônios gonadais, pelo poder estatístico limitado devido a pequenas coortes e pela heterogeneidade entre os indivíduos nos fatores genéticos e ambientais que influenciam a obesidade . O uso de modelos de camundongos permite superar algumas dessas limitações e avaliar as contribuições relativas desexocromossomos e hormônios gonadais às diferenças sexuais.
Uma abordagem tradicional usada em modelos de camundongos para identificar a causa desexodiferenças é avaliar a ação dos hormônios gonadais após a puberdade [70]. Camundongos machos e fêmeas adultos são gonadectomizados e avaliados para verificar se a diferença sexual original foi eliminada. Em caso afirmativo, a substituição de hormônios por uma bomba implantada ou injeção diária é realizada e os camundongos são observados para determinar se a diferença sexual original foi restaurada. Os estudos de acompanhamento podem incluir a identificação do receptor hormonal que medeia o efeito, o que pode ser feito por meio de inibição química ou genética da função do receptor hormonal. Para diferenças sexuais que ocorrem antes da puberdade, ou que não são alteradas pela gonadectomia, o papel dos picos de testosterona que ocorrem pré ou pós-natal pode ser estudado. Para um desempenho significativo e interpretação de estudos que manipulam hormônios gonadais, muitos fatores devem ser considerados e revisados em outros lugares [70]. Se as diferenças hormonais gonadais não puderem explicar completamente uma diferença sexual, o efeito potencial do complemento dos cromossomos sexuais deve ser considerado.
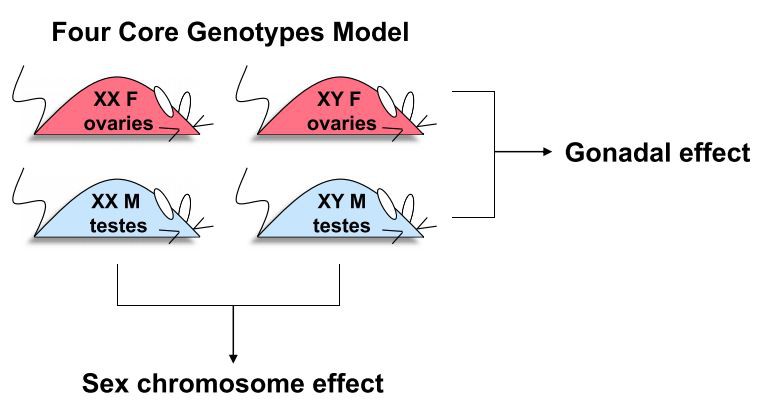
Um modelo de camundongo que foi projetado especificamente para analisar os efeitos dos hormônios gonadais, bem comosexocromossomos, é o rato Four Core Genotypes (FCG). O modelo envolve a realocação do gene Sry, que promove o desenvolvimento dos testículos, do cromossomo Y para um autossomo, de modo que o sexo gonadal possa segregar independentemente do complemento cromossômico sexual [70,71]. A posição do gene Sry em um autossomo não altera os níveis de andrógenos pré-natais ou adultos [72]. Estudos realizados com camundongos FGC envolvem a comparação de quatro genótipos, que embaralham os componentes cromossômicos e gonadais do sexo para gerar camundongos XX com ovários ou testículos e camundongos XY com ovários ou testículos (referidos, respectivamente, como XX F, XX M, XYF e XYM). Uma comparação dois a dois desses quatro genótipos permite a identificação de efeitos que são ditados pelo tipo gonadal ousexotipo de cromossomo (Figura 1). Para eliminar a contribuição dos hormônios gonadais circulantes, os camundongos FCG são frequentemente estudados após a gonadectomia quando adultos.
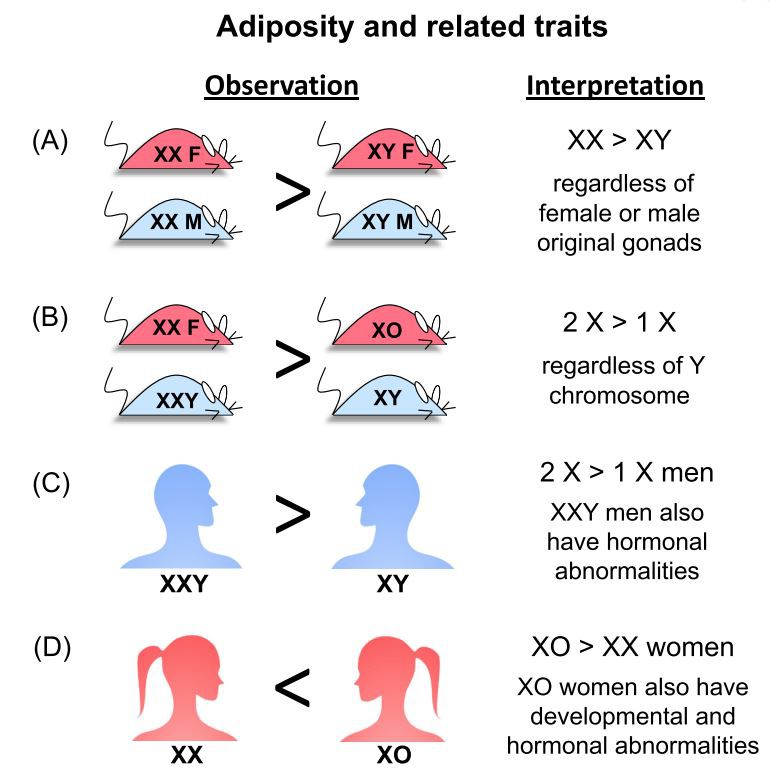
Usando o modelo FCG, os efeitos desexocomplemento cromossômico em vários traços metabólicos foram identificados, incluindo obesidade, perfil lipídico plasmático, ingestão alimentar e hipertensão [73-77]. Em camundongos C57BL/6 FCG que foram gonadectomizados como adultos para remover os efeitos agudos dos hormônios gonadais, camundongos com cromossomos XX versus XY (independentemente das gônadas masculinas ou femininas presentes originalmente) ganharam peso mais rapidamente com ração ou dieta rica em gordura e acumularam mais peso corporal. gordura, particularmente no depósito de gordura subcutânea inguinal (Figura 2) [73]. O aumento do ganho de peso em camundongos XX em comparação com XY foi promovido, pelo menos em parte, pelo aumento da ingestão de alimentos por camundongos XX, especificamente durante a fase leve do ciclo circadiano [74]. Como animais noturnos, os camundongos consomem aproximadamente 70% de suas calorias durante a fase escura e descansam e lancham (30% do total de calorias) durante a fase clara. O aumento da ingestão de alimentos por camundongos XX na fase leve foi devido à alimentação antecipada iniciada cerca de 1,5 h antes de seus equivalentes XY [74]. Além do aumento do acúmulo de tecido adiposo, camundongos XX alimentados com uma dieta rica em gordura por 16 semanas desenvolveram condições relacionadas à obesidade, como fígado gorduroso, níveis elevados de colesterol total no sangue e níveis elevados de insulina [73]. É provável que esses distúrbios metabólicos sejam secundários ao aumento do acúmulo de gordura em camundongos XX alimentados com dieta rica em gordura, uma vez que não são observados em camundongos XX alimentados com dieta alimentar.
Os dados dos camundongos FCG mostraram claramente um efeito dos cromossomos XX comparados aos cromossomos XY na adiposidade e morbidades relacionadas à obesidade. Mas esses estudos sozinhos não distinguiram entre um efeito da dosagem do cromossomo X (dois versus um X) ou um efeito da presença ou ausência do cromossomo Y. A análise de modelos de camundongos com genótipos de cromossomos sexuais adicionais tornou possível identificar o efeito relevante do cromossomo sexual. Ao fazer uso de um cromossomo Y incomum com duplicações de sequência na região pseudoautossômica (conhecida como modelo XY*, [71]), camundongos com cromossomos XX, XY, XO e XXY foram avaliados quanto ao peso corporal e adiposidade. Os resultados mostraram que a presença de dois cromossomos X (camundongos XX e XXY) levou a maior peso corporal/gordura do que um cromossomo X (XY e XO); a presença do cromossomo Y não teve influência (Figura 2) [73].

haste de cistache
6. EFEITOS CROMOSSÔMICOS SEXUAIS NOS NÍVEIS LIPÍDICOS
Além da adiposidade,sexocomplemento cromossômico em camundongos e humanos influencia os níveis de lipídios plasmáticos. Níveis elevados de colesterol plasmático total e de subclasses de lipoproteínas específicas têm associações epidemiológicas bem conhecidas com doenças cardiovasculares. Em um nível geral, elevações nas lipoproteínas de baixa densidade (LDL) e reduções nos níveis de lipoproteínas de alta densidade (HDL) estão associadas ao aumento do risco de doença cardiovascular [78]. Os resultados atuais sugerem que componentes específicos do perfil lipídico são influenciados independentemente pela dosagem do cromossomo X, presença do cromossomo Y e hormônios gonadais; as diferenças de sexo observadas são provavelmente um composto de todas essas contribuições. Por exemplo, os hormônios gonadais parecem regular o metabolismo das lipoproteínas, pois as mulheres na pré-menopausa tendem a ter níveis mais altos de HDL e níveis mais baixos de LDL do que os homens, e na pós-menopausa, os perfis de lipoproteínas tornam-se mais semelhantes aos dos homens (revisado na Ref. [18]) . A evidência dos efeitos do cromossomo Y vem da demonstração de que as variações genéticas no cromossomo Y estão associadas a perfis de lipoproteínas em homens [79,80] e camundongos [81]. Além disso, estudos com o modelo de camundongo FCG revelaram efeitos da dosagem do cromossomo X nos níveis de colesterol HDL, enquanto os hormônios gonadais tiveram efeitos nos níveis de triglicerídeos e ácidos graxos [18,77].
7. DIFERENÇAS SEXUAIS NA INFLAMAÇÃO E IMUNOMETABOLISMO
A obesidade é uma doença inflamatória, e foi demonstrado em camundongos que machos e fêmeas diferem na resposta inflamatória que ocorre na obesidade induzida por dieta [82]. As diferenças sexuais na resposta inflamatória que é desencadeada pela dieta rica em gordura em camundongos incluem aumento da infiltração no tecido adiposo com macrófagos M1 (CD11c+) em machos, mas macrófagos M2 (CD11ce) em fêmeas e níveis aumentados de citocinas inflamatórias em machos em comparação com fêmeas. 83]. Estudos de transplante de medula óssea demonstraram que a resposta inflamatória dependente do sexo está relacionada a um dimorfismo sexual intrínseco à célula na composição ou ativação de populações de células-tronco hematopoiéticas [83].
As doenças autoimunes estão entre as maissexo- tendenciosa de todas as doenças, e 80 por cento dos pacientes autoimunes são mulheres [84]. A obesidade é um fator de risco para doenças auto-inflamatórias e autoimunes, incluindo lúpus eritematoso sistêmico, diabetes tipo 1, artrite reumatóide e psoríase [85]. As ligações mecanicistas prováveis entre obesidade e disfunção autoimune incluem alterações dependentes do sexo nos níveis de adipocinas produzidas por adipócitos (por exemplo, leptina, resistina, adiponectina, visfatina) e produção de citocinas inflamatórias (por exemplo, fator de necrose tumoral-a, interleucina {{ 7}}). Tanto os hormônios gonadais quanto a dosagem do cromossomo X foram implicados no viés feminino na doença autoimune [86]. Consistente com os efeitos dos hormônios gonadais, o viés sexual na doença autoimune é mais evidente após a puberdade. Estrogênios e andrógenos exercem influências distintas sobre a produção de citocinas e diferenciação de células T. A testosterona é supressora da resposta imune adaptativa e inata, enquanto o estrogênio pode promover respostas inflamatórias [87,88]. Uma interação entre a composição microbiana do intestino no início da vida e os níveis de hormônios gonadais foi identificada no diabetes tipo 1 em camundongos diabéticos não obesos [89]. Neste modelo, as bactérias comensais no intestino elevaram os níveis séricos de testosterona em machos, o que foi protetor contra o diabetes tipo 1. A transferência de populações microbianas intestinais de machos adultos para fêmeas imaturas resultou em níveis elevados de testosterona, redução da inflamação das ilhotas pancreáticas e proteção contra diabetes tipo 1. Esses efeitos eram dependentes da atividade do receptor de andrógeno.
Além dos efeitos dos hormônios gonadais na autoimunidade,sexocomplemento cromossômico provavelmente desempenha um papel. Usando o modelo de camundongo FCG para estudar encefalomielite autoimune experimental (relevante para esclerose múltipla) e lúpus espontâneo, a doença foi mais grave em camundongos XX em comparação com camundongos XY com gônadas femininas [90e92]. Estudos de metilação do DNA sugeriram que a impressão materna versus paterna de genes do cromossomo X poderia contribuir para asexodiferenças na encefalite imune experimental [93]. A dosagem do gene do cromossomo Y também tem sido implicada na doença autoimune. Por exemplo, a variação genética natural no número de cópias de genes multicópia no cromossomo Y está associada à suscetibilidade à encefalomielite alérgica experimental e miocardite experimental no camundongo [94]. O estudo de linhagens de camundongos com cromossomo Y (que possuem o cromossomo Y de uma linhagem de camundongos endogâmicos no fundo de outra linhagem pura) revelou uma ligação entre o número de cópias de dois genes específicos do cromossomo Y e a expressão gênica em células imunes [94]. O papel das sequências do cromossomo Y como regulador de expressão gênica de ação trans pode contribuir para o dimorfismo sexual na doença autoimune. No entanto, a interpretação de tais achados é complexa. Por um lado, eles podem indicar que o cromossomo Y pode ser parcialmente responsável por conferir as diferenças sexuais observadas na suscetibilidade à doença autoimune. Por outro lado, foi sugerido que a expressão gênica do cromossomo Y atua como um “balanceador” dos efeitos do cromossomo X. Nessa visão, a expressão de genes do cromossomo Y torna os machos mais parecidos com as fêmeas, de modo que a dosagem alterada do gene do cromossomo Y pode derrubar a balança e influenciar as diferenças sexuais em doenças autoimunes e outras características [95].
8. MECANISMOS POTENCIAIS PARA EFEITOS CROMOSSÔMICOS SEXUAIS NO METABOLISMO
Existem vários mecanismos que podem estar subjacentes aos efeitos dasexocomplemento cromossômico na obesidade, metabolismo lipídico, autoimunidade e outras características. A presença de cromossomos XX ou XY influencia profundamente o caminho do desenvolvimento e estabelece uma diferença vitalícia entre os sexos nos níveis de hormônios gonadais. Tanto os hormônios gonadais quanto os cromossomos sexuais influenciam a expressão gênica, o que provavelmente está por trás das diferenças fenotípicas observadas entre machos e fêmeas. Os primeiros estudos de expressão gênica em camundongos machos e fêmeas de um cruzamento genético de duas linhagens endogâmicas revelaram diferenças macho/fêmea na expressão gênica no tecido adiposo, fígado e músculo esquelético (milhares de genes), bem como no cérebro (centenas de genes). [96]. Este estudo também forneceu evidências para a regulação global de subconjuntos de genes que foram diferencialmente expressos entre ossexos. Um estudo subsequente na mesma população intercruzada de camundongos revelou correlações entre gordura corporal e níveis lipídicos e módulos de expressão gênica específicos do sexo no tecido adiposo e no fígado; muitos dos módulos demonstraram ser regulados por hormônios gonadais [97]. Estudos adicionais revelaram influências dos hormônios gonadais nos perfis transcricionais de depósitos de tecido adiposo subcutâneo e visceral [31,36].
Modelos de camundongos também revelaram os efeitos dos cromossomos sexuais na expressão gênica. É importante notar que os cromossomos sexuais influenciam a expressão de centenas de genes autossômicos e alguns desses efeitos são modulados pela presença do gene determinante do testículo, Sry [98e100]. Os microRNAs (miRNAs), que modulam os níveis de expressão gênica interagindo com espécies específicas de mRNA para aumentar sua degradação ou interferir na tradução, também são influenciados pelo sexo. Usando o modelo de camundongo FCG para analisar os efeitos do sexo gonadal e cromossômico, o perfil geral de expressão de miRNA mostrou um viés para maior expressão no tecido adiposo gonadal masculino em comparação com o feminino [101]. Esse viés foi normalizado após a gonadectomia, indicando um papel dos hormônios gonadais circulantes na modulação dos níveis de miRNA. Em camundongos alimentados com uma dieta rica em gordura, os níveis de miRNA foram maiores em camundongos com complemento cromossômico XX versus XY. Assim, há um efeito composto de hormônios gonadais e cromossomos sexuais na expressão de miRNAs e, presumivelmente, nos mRNAs regulados por esses miRNAs.
A recent analysis of human transcriptome data from the GTEx project is consistent with mouse data in detecting thousands of genes that are differentially expressed in male and female tissues [102]. The GTEx project includes RNA-seq data from >50 tecidos de centenas de homens e mulheres [103]. A maioria dos genes que apresentaram diferenças sexuais nos níveis de expressão exibiram essas diferenças em um ou alguns tecidos [102]. Por outro lado, 16 genes do cromossomo X tiveram diferenças sexuais em pelo menos seis tecidos, sugerindo efeitos generalizados. Dos tecidos encontrados em machos e fêmeas, a expressão gênica mais diferenciada por sexo ocorreu no tecido mamário, consistente com a fisiologia sexualmente dimórfica e a estrutura do tecido mamário [102].
É simples imaginar como os hormônios gonadais podem influenciar a expressão gênica em todo o genoma, mas menos intuitivo entender como as diferenças no complemento dos cromossomos sexuais podem alterar a expressão dos genes nos autossomos. A presença de dois cromossomos X em uma célula confere propriedades únicas que não estão presentes em uma célula XY. Nas células XX, um cromossomo X é transcricionalmente silenciado em células fora da linhagem germinativa para reduzir a expressão da maioria dos genes do cromossomo X, de modo que os níveis sejam comparáveis entre as células XX e XY. No entanto, alguns genes do cromossomo X "escapam" da inativação e permanecem transcricionalmente ativos em ambos os cromossomos X nas células XX. É importante ressaltar que os genes que escapam da inativação do X são amplamente conservados entre humanos e camundongos [104e108].
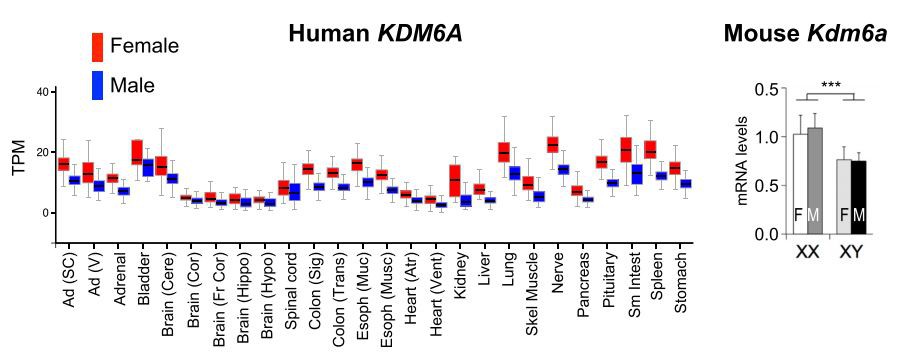
Os genes fugitivos de inativação do X apresentam expressão aumentada em tecidos de mulheres em comparação com homens, inclusive em tecidos metabólicos como tecido adiposo e fígado. Um perfil de expressão em homens e mulheres para um gene fugitivo do cromossomo X representativo (KDM6A) é mostrado na Figura 3. O gene de camundongo correspondente (Kdm6a) exibe níveis de expressão aumentados em XX em comparação com camundongos XY FGC, mostrando que esse efeito é determinado pelo sexo complemento cromossômico em vez de hormônios gonadais (Figura 3). Estima-se que 3,6% dos genes do cromossomo X do camundongo escapam da inativação, e esses mesmos genes mais outros (aproximadamente 15% dos genes do cromossomo X) escapam da inativação em humanos [104e108]. Alguns genes X fugitivos têm genes parceiros que foram retidos no cromossomo Y, e o escape da inativação pode ajudar a normalizar a expressão desses genes entre as células XX e XY. No entanto, muito mais genes do cromossomo X escapam da inativação do que parceiros no cromossomo Y [107]. Os genes X escapee codificam proteínas que podem influenciar amplamente a expressão gênica, incluindo enzimas modificadoras de histonas, proteínas de iniciação da tradução e RNA helicases, para citar algumas. Também existem diferenças entre as células XX e XY devido à impressão do pai de origem. Imprinting genômico é o DNA hereditário ou metilação de histonas em regiões específicas dos cromossomos que leva ao silenciamento transcricional. Imprints são estabelecidos na linhagem germinativa da mãe ou do pai e passados para a prole de tal forma que o alelo de apenas um dos pais será expresso na prole. As células XX recebem um cromossomo X do pai e da mãe, enquanto uma célula XY recebe um X exclusivamente da mãe. Assim, apenas as células XX sofrem imprinting do cromossomo X paterno, o que pode levar a diferenças na expressão gênica em XX em comparação com as células XY. Para uma discussão mais extensa desses mecanismos, o leitor deve consultar excelentes revisões recentes [47,71].
9. PERSPECTIVAS FUTURAS
Propomos que não compreenderemos completamente muitos aspectos do metabolismo até compreendermos as diferenças sexuais no metabolismo. Isso inclui diferenças entre mulheres e homens no risco e desenvolvimento de obesidade e na manifestação de morbidades relacionadas. A identificação dessas diferenças pode revelar como um sexo está protegido de desfechos específicos de doenças em comparação com o outro e sugerir novas possibilidades de prevenção e tratamento para ambos os sexos. Abordagens de pesquisa que consideram os componentes dos efeitos de viés sexual, incluindo diferenças ditadas pelo tipo de gônada e pelo complemento dos cromossomos sexuais, fornecerão o entendimento mais completo. O estudo de modelos de camundongos com combinações únicas de cromossomos sexuais e humanos com variações naturais de cromossomos sexuais já começaram a sugerir efeitos importantes dos cromossomos sexuais na obesidade, metabolismo lipídico e inflamação. Uma maior compreensão exigirá uma elucidação mais completa das diferenças moleculares conferidas pela presença de complementos cromossômicos XX ou XY. O atual reconhecimento do sexo como uma importante variável biológica a ser considerada na pesquisa [109e111] provavelmente fornecerá uma nova (e bem-vinda) motivação para impulsionar o campo.

REFERÊNCIAS
[1]Voskuhl, R., 2011. Diferenças sexuais em doenças autoimunes. Biologia das Diferenças Sexuais 2(1):1.
[2]Klein, SL, Flanagan, KL, 2016. Diferenças sexuais nas respostas imunes. Nature Reviews Immunology 16(10):626e638.
[3]Jaillon, S., Berthenet, K., Garlanda, C., 2017. Dimorfismo sexual na imunidade inata. Revisões Clínicas em Alergia e Imunologia.
[4]Aswat, KA, 2017. Disparidades de gênero na osteoporose. Journal of Clinical Medicine Research 9(5):382e387.
[5] Laws, KR, Irvine, K., Gale, TM, 2018. Diferenças sexuais na doença de Alzheimer. Opinião Atual em Psiquiatria 31(2):133e139.
[6] Rainville, JR, Tsyglakova, M., Hodes, GE, 2017. Decifrando diferenças sexuais no sistema imunológico e depressão. Fronteiras em Neuroendocrinologia.
[7]Werling, DM, Geschwind, DH, 2013. Diferenças sexuais nos transtornos do espectro do autismo. Current Opinion in Neurology 26(2):146e153.
[8]Jurado-Coronel, JC, Cabezas, R., Ávila Rodríguez, MF, Echeverria, V., García- Segura, LM, Barreto, GE, 2017. Diferenças sexuais na doença de Parkinson: características sobre sintomas clínicos, tratamento resultado, hormônios sexuais e genética. Fronteiras em Neuroendocrinologia.
[9]Li, R., Ma, X., Wang, G., Yang, J., Wang, C., 2016. Por que diferenças sexuais na esquizofrenia? Journal of Translational Neuroscience 1(1):37e42.
[10]Regitz-Zagrosek, V., 2012. Diferenças de sexo e gênero na saúde. Relatórios EMBO 13(7):596e603.
[11]Dobyns, W., 2006. O padrão de herança de traços ligados ao X não é dominante ou recessivo, apenas ligado ao X. Acta Pediatrica 95(0):11e15.
[12]Shah, RR, Bird, AP, 2017. Mutações de MeCP2: progresso no sentido de compreender e tratar a síndrome de Rett. Medicina do Genoma 9(1):17.
[13]Mauvais-Jarvis, F., Clegg, DJ, Hevener, AL, 2013. O papel dos estrogênios no controle do balanço energético e da homeostase da glicose. Revisões Endócrinas 34(3):309e338.
[14] Karastergiou, K., Smith, SR, Greenberg, AS, Fried, SK, 2012. Diferenças sexuais nos tecidos adiposos humanos e a biologia da forma da pêra. Biologia das Diferenças Sexuais 3(1):13.
[15]Karpe, F., Pinnick, KE, 2015. Biologia do tecido adiposo da parte superior e inferior do corpo liga-se aos fenótipos do corpo inteiro. Nature Reviews Endocrinology 11(2): 90e100.
[16]Karastergiou, K., Fried, SK, 2017. Mecanismos celulares que conduzem as diferenças sexuais na biologia do tecido adiposo e na forma do corpo em modelos de humanos e camundongos. Avanços em Medicina Experimental e Biologia 1043:29e51.
[17]Mundi, MS, Koutsari, C., Jensen, MD, 2014. Efeitos do aumento da disponibilidade de ácidos graxos livres no armazenamento de ácidos graxos no tecido adiposo em homens. The Journal of Clinical Endocrinology & Metabolism 99(12): E2635eE2642.
[18]Link, JC, Reue, K., 2017. Base genética para diferenças sexuais na obesidade e metabolismo lipídico. Revisão Anual de Nutrição 37(1):225e245.
[19]Pulit, SL, Karaderi, T., Lindgren, CM, 2017. Dimorfismos sexuais em loci genéticos ligados à distribuição de gordura corporal. Relatórios de Biociência 37(1).
[20]Bouchard, C., Pérusse, L., Leblanc, C., Tremblay, A., Thériault, G., 1988. Herança da quantidade e distribuição da gordura corporal humana. International Journal of Obesity 12(3):205e215.







