Memória imune inata e adaptativa: um continuum evolutivo na resposta do hospedeiro aos patógenos (Parte 1)
Jun 08, 2022
Para saber mais informações entre em contatodavid.wan@wecistanche.com
Memória imunológicaé uma característica evolutiva importante que melhora a sobrevivência do hospedeiro após a reinfecção, a memória é uma característica reconhecida dentro dos braços inato e adaptativo do sistema imunológico. Embora os mecanismos e propriedades através dos quais a memória imune inata e adaptativa são induzidas sejam distintos, eles conspiram para melhorar a defesa do hospedeiro contra patógenos. Aqui, propomos que a memória imune inata, ou "imunidade treinada", é uma forma primitiva de adaptação na defesa do hospedeiro, resultante do rearranjo da estrutura da cromatina, que fornece uma resposta aumentada, mas não específica, à reinfecção. Em contraste, a memória imune adaptativa é mais avançada, com maior magnitude de resposta mediada por mudanças epigenéticas, bem como especificidade mediada porrecombinação genética. Um modelo integrador de memória imunológica é importante para uma ampla compreensão da defesa do hospedeiro e para identificar as abordagens mais eficazes para modulá-la em benefício de pacientes com infecções e doenças imunomediadas.

Clique aqui para saber mais sobre Cistanche
Imunidade Inata e Adaptativa
Classicamente, a imunidade do hospedeiro é dividida em respostas imunes inatas e adaptativas. O primeiro reage de forma rápida e não específica aos patógenos, enquanto o segundo responde de maneira mais lenta, mas específica, com a geração de memória imunológica de longa duração (Farber et al., 2016). Essa dicotomia ditou o último meio século depesquisa imunológica, e um grande número de estudos definiu os substratos celulares e moleculares de cada um desses dois principais componentes da defesa do hospedeiro. A imunidade inata é mediada por populações de células imunes inatas, como células mieloides, células natural killer (NK) e células linfoides inatas (mas também células não imunes em circunstâncias específicas), bem como por sistemas humorais antigos, como defensinas e complemento. . A imunidade adaptativa é um traço evolutivo relativamente novo baseado na família de imunoglobulinas e células como linfócitos B e T em vertebrados com mandíbula (Danilova, 2012) e em receptores de linfócitos variáveis (VLR) compostos por segmentos repetidos de leucina (LRR) em vertebrados sem mandíbula (Boehm et al., 2012).
Durante uma infecção, a imunidade inata é a primeira a ser acionada (a reação inflamatória), não levando mais do que minutos a horas para ser totalmente ativada (Netea et al., 2017). Isso é crucial para a defesa do hospedeiro na primeira fase de uma nova infecção. Enquanto a imunidade inata é geralmente capaz de eliminar os patógenos de forma eficiente, a eliminação inicial da infecção pode falhar devido ao alto número ou virulência depatógenos invasores. Nessas situações, os linfócitos e os mecanismos imunes adaptativos são ativados, o que permite o reconhecimento específico e a eliminação do patógeno. O estabelecimento da imunidade adaptativa precisa de 1-2 semanas e é importante para a defesa do hospedeiro durante as últimas fases da infecção e durante as infecções secundárias devido à sua capacidade de "lembrar" e responder de forma mais eficaz à reestimulação (Farber et al., 2016) .
Os processos imunológicos inatos e adaptativos foram inicialmente vistos como respostas relativamente compartimentadas no tempo, mas as pesquisas nas últimas duas décadas demonstraram claramente fortes ligações e uma rede eficiente entre eles. A ativação da resposta imune adaptativa e a indução da memória imune clássica nos linfócitos são dependentes do sistema imune inato, em particular das células apresentadoras de antígeno, como as células dendríticas. Os efeitos a jusante da ativação de linfócitos são então exercidos pela amplificação das respostas imunes inatas, como fagocitose e morte de patógenos por certas células imunes inatas. Duas propriedades que discriminam entre imunidade inata e adaptativa são, por um lado, a especificidade e, por outro, a capacidade de construir memória imunológica de longa duração. As respostas imunes inatas são tradicionalmente consideradas inespecíficas e sem capacidade de adaptação, enquanto as respostas imunes adaptativas reconhecem com grande precisão diferentes patógenos usando processos de recombinação de genes na família de genes de imunoglobulinas e, posteriormente, constroem memória imunológica (Danilova, 2012) (Figura 1). O conceito de que a imunidade inata é inespecífica foi desafiado pela descoberta de receptores de reconhecimento de padrões (PRR). Esses receptores expressos em uma variedade de células dentro do sistema imune inato reconhecem componentes específicos demicroorganismos, e a combinação de PRRs expressos por uma célula imune pode levar ao reconhecimento parcialmente específico do tipo de microrganismo encontrado: por exemplo, células imunes inatas reconhecem a diferença entre uma bactéria Gram-negativa e uma Gram-positiva, mas não entre duas bactérias próximas. espécies ou linhagens relacionadas (Medzhitov e Janeway, 2000). Não discutiremos o progresso na compreensão do reconhecimento de patógenos por meio de PRRs nesta revisão, pois este é o assunto de muitas visões recentes excelentes na literatura (por exemplo, O'Neill et al., 2013).
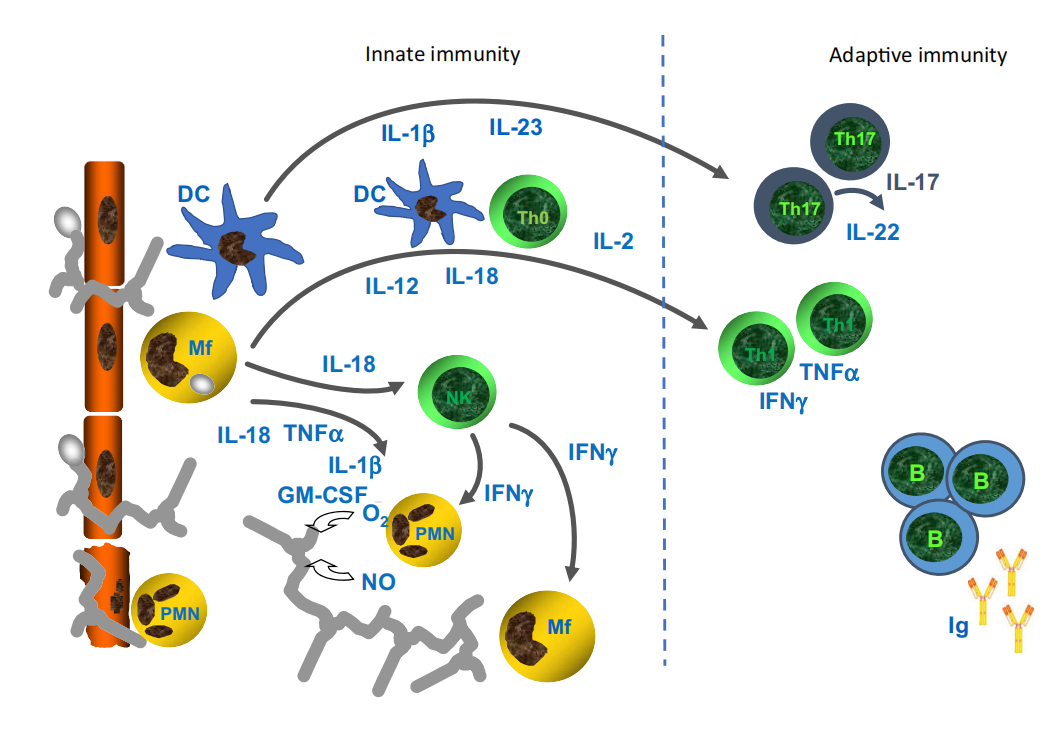
Figura 1. Respostas imunes inatas versus adaptativas
Durante as primeiras horas e dias de infecção, a invasão por patógenos induz a ativação de células imunes inatas como macrófagos, monócitos ou células NK ou fatores humorais como complemento. Essas vias ativam fortemente uma reação inflamatória e eliminam patógenos (imunidade inata). Nos poucos casos em que a infecção não é eliminada, os patógenos são ingeridos e processados por células apresentadoras de antígenos, seguido de apresentação de antígenos e estimulação da ativação específica deLinfócitos T e B. Por sua vez, isso leva à expansão clonal e ativação de mecanismos efetores (por exemplo, a liberação de citocinas e imunoglobulinas) (imunidade adaptativa).
Aqui, vamos nos concentrar na segunda propriedade que discrimina os mecanismos de defesa do hospedeiro inato e adaptativo: a indução da memória imunológica. Em contraste com a literatura inicial, um crescente corpo de evidências mostra que as respostas imunes inatas exibem características adaptativas (Bowdish et al., 2007; Netea et al., 2011). Em plantas e invertebrados que não possuem imunidade adaptativa, foi relatada proteção sustentada contra a reinfecção (Kurtz, 2005). Estudos em mamíferos demonstraram que há proteção cruzada contra infecções com diferentes patógenos (Quintin et al., 2014), enquanto estudos experimentais de camundongos desprovidos de células imunes adaptativas funcionais mostraram proteção parcial em certos modelos de vacinação (Bistoni et al., 1986; não pode Wout et al, 1992). É assim aparente que a imunidade inata pode ser modulada por encontros anteriores com micróbios ou produtos microbianos, e esta propriedade tem sido denominada "imunidade treinada" e representa uma memória imune inata de facto.
No entanto, existem mecanismos moleculares distintos que medeiam os dois tipos de memória imunológica. Com base em argumentos moleculares, imunológicos e evolutivos, propomos que a memória imune inata é uma forma primitiva de memória imune presente em todos os organismos vivos, enquanto a memória imune adaptativa é uma forma avançada de memória imune que representa uma inovação evolutiva em vertebrados. Com base nas propriedades complementares dos dois tipos de memória imunológica e em uma série de argumentos biológicos descritos abaixo, argumentamos nesta Perspectiva que o desenvolvimento da memória imunológica inata e adaptativa representa um continuum evolutivo. Também propomos que essas duas formas são duas etapas evolutivas para o desenvolvimento de mecanismos eficazes de adaptação a um ambiente repleto de agentes potencialmente patogênicos.microorganismos.
Memória imunológica como traço evolutivo adaptativo
O dogma de que a memória imunológica está confinada ao sistema imune adaptativo enfrenta uma dificuldade conceitual quando considerado de uma perspectiva evolutiva. Que a memória imunológica é vantajosa do ponto de vista evolutivo é bem ilustrada por doenças antigas mortais como a varíola: enquanto a mortalidade era historicamente de 20 por cento -60 por cento para as primeiras infecções, os indivíduos tornaram-se completamente imunes à doença depois disso (Riedel, 2005 ). Portanto, é difícil imaginar que a memória imunológica evoluiu apenas em vertebrados, que representam aproximadamente 1% -2 por cento das espécies vivas (Gourbal et al., 2018). Em contraste, outras importantes características vantajosas, como visão, evoluíram independentemente várias vezes durante a evolução de vários grupos de animais (a chamada "evolução convergente") (Gehring, 2004). Interessantemente,memória imunológicadentro da linhagem de vertebrados evoluiu não apenas uma, mas duas vezes. Primeiro, o desenvolvimento da memória baseada em VLR nos peixes sem mandíbula (como a lampreia) e, segundo, o desenvolvimento da memória baseada em LG (que também é a base para o desenvolvimento da memória de linfócitos B e T) em todos os outros vertebrados com mandíbula. Que haveria dois eventos separados levando à memória imunológica em vertebrados (Cooper e Alder, 2006), embora completamente ausente em todos os outros metazoários, é muito improvável.

Figura 2. Memória imune versus adaptação imune
A memória imunológica é definida como um estado alterado do sistema imunológico de um hospedeiro após infecção aguda (ou vacinação), levando a uma resposta mais eficaz contra a reinfecção. É importante ressaltar que durante a indução da memória imunológica, entre a primeira infecção e a reinfecção, o estado imunológico retorna funcionalmente a um estado basal baixo, enquanto a capacidade de responder mais forte à reestimulação é impressa no nível epigenético (A). Em contraste, a adaptação é definida como a mudança de longo prazo na resposta imune determinada por uma mudança constante nas condições ambientais, ou devido a um insulto crônico (por exemplo, uma infecção crônica), levando a um novo estado funcional. É importante ressaltar que o estado imunológico funcional durante a adaptação não retorna ao estado basal baixo existente antes do insulto (B).
Em consonância com isso, um grande número de estudos de imunologia vegetal tem demonstrado que a defesa do hospedeiro da planta inclui características adaptativas, uma resposta denominada Resistência Adquirida Sistêmica (SAR) (Jaskiewicz et al., 2011; Kachroo e Robin, 2013; Reimer-Michalski e Conrado, 2016). Os mecanismos moleculares e mediadores bioquímicos da SAR são amplamente conhecidos (Kachroo e Robin, 2013), com a religação da defesa do hospedeiro baseada na epigenética sendo sugerida para desempenhar um papel central (Luna e Ton, 2012). crença de que a imunidade inata dos invertebrados carece de traços de memória (Kurtz, 2005). Propriedades adaptativas de respostas imunes inatas foram relatadas em várias linhagens de invertebrados; por exemplo, omicrobiotademonstrou induzir memória imune inata para proteger mosquitos contra Plasmodium (Rodrigues et al, 2010), e o inseto social Bombus Terrestris para exibir memória imune inata contra três patógenos diferentes (Sadd e Schmid-Hempel, 2006), e a tênia Schistocephalus solidus para induzir memória no crustáceo copépode (Kurtz e Franz, 2003), e a memória imune inata é um mecanismo de defesa em caracóis (Pinaud et al, 2016). Esses estudos foram complementados por dados em vertebrados mostrando que é possível induzir proteção parcial contra reinfecção em modelos murinos experimentais mesmo na ausência de respostas imunes adaptativas funcionais (Bistoni et al.,1986; can't Wout et al.,1992 ). Além disso, estudos epidemiológicos mostraram proteção heteróloga por vacinas humanas contra um amplo espectro de infecções (Benn et al., 2013), com mecanismos provavelmente independentes das respostas imunes adaptativas clássicas. Portanto, é razoável concluir que a memória imunológica pode ser encontrada não apenas em vertebrados, mas também em plantas e animais inferiores (Kurtz, 2005; Ne-tea et al., 2011) que não abrigam um sistema imunológico adaptativo clássico.

Memória imune inata e adaptativa: um processo evolutivo
Se esses dados defendem fortemente a presença de memória imunológica em todos os grupos de organismos superiores, como isso pode ser definido? Uma definição simples é que a memória imunológica se refere à capacidade do sistema imunológico de responder mais rápida e eficazmente a um patógeno. Essa definição abrange todos os processos descritos como memória imunológica em plantas, invertebrados e vertebrados, embora não discrimine entre as diferenças de ação observadas em vários grupos de organismos. Em uma revisão recente, Pradeu e Du Pasquier (2018) propõem um modelo multidimensional de memória imunológica, no qual discriminam nada menos que seis variedades de memória imunológica: memória adaptativa clássica em vertebrados, memória imunológica de células NK, imunidade treinada em células mieloides , priming em invertebrados, memória imunológica em plantas (por exemplo, SAR) e memória baseada em Crispr/Cas em bactérias e archaea (Pradeu e Du Pasquier, 2018). Essas formas de memória imunológica diferem em suas propriedades com base em várias características básicas da resposta: força, velocidade, extinção (reversão ao estado basal), duração e especificidade. No entanto, embora essa classificação seja útil para entender a presença onipresente da memória imunológica em todos os organismos vivos, acreditamos que issocompartimentalizaçãoda memória imunológica não reflete o substrato molecular, biológico e funcional comum das características da memória em diferentes organismos.
Nesta Perspectiva, propomos um modelo unificador de memória imunológica que se baseia em dois conceitos:
Há uma diferença conceitual entre duas formas de adaptação imune: memória imune e diferenciação imune.
Um continuum evolutivo liga a memória imune inata e adaptativa.
O primeiro conceito que precisa ser definido é representado pela diferença entre memória imune e adaptação imune. Definimos memória imunológica como um estado alterado do sistema imunológico de um hospedeiro após infecção aguda (ou vacinação), levando a uma resposta mais eficaz contra a reinfecção. É importante ressaltar que durante a indução da memória imunológica, entre a primeira infecção e a reinfecção, o estado imunológico retorna funcionalmente a um estado basal baixo, enquanto a capacidade de responder mais forte à reestimulação é impressa no nível epigenético (Figura 2A). Em contraste, definimos a diferenciação imune como uma forma de adaptação por meio de mudanças de longo prazo no programa funcional de um sistema (incluindo a resposta imune), determinada por uma mudança constante nas condições ambientais ou devido a um insulto crônico (por exemplo, uma doença crônica). infecção), levando a um novo estado funcional. É importante ressaltar que o estado imunológico funcional durante a diferenciação não retorna ao estado basal baixo existente antes do insulto (Figura 2B). Existem muitas situações biológicas caracterizadas pela adaptação através da diferenciação imune: uma dessas situações pode ser induzida, por exemplo, por mudanças estáveis na microbiota intestinal, que é conhecida por induzir efeitos de longo prazo nas respostas imunes locais. O processo de diferenciação imunológica é objeto de muitas outras excelentes revisões, e não será o foco desta Perspectiva.
Outra distinção importante a ser feita é entre priming e memória. Priming também é um termo que tem sido usado para descrever respostas aumentadas a um estímulo secundário, no entanto, este é frequentemente um processo agudo que não envolve efeitos de memória de longo prazo. Por exemplo, durante a infecção aguda da malária, há uma conhecida hiper-responsividade das células imunes a microrganismos Gram-negativos que podem levar a sintomas agudos graves: as células imunes são preparadas para responder agudamente com maior liberação de citocinas. No entanto, isso não implica uma resposta de memória que persistiria por meses ou anos.
Aqui, vamos nos concentrar no conceito de memória imunológica, que acreditamos caracteriza todos os organismos vivos. Propomos que existe um continuum evolutivo entre a memória imune inata e adaptativa com base em duas propriedades fundamentais mediadas por mecanismos distintos:
● Aumento da magnitude e cinética do sistema imunológico
respostas após a reinfecção, que é mediada por processos epigenéticos e caracteriza a memória imune inata e adaptativa (presente em todos os organismos)
● Especificidade das respostas de memória, mediadas por gene
recombinação, uma propriedade específica da memória imune adaptativa (descrita até agora apenas em vertebrados)

Memória imune inata
Enquanto na imunidade de vertebrados há muito se assume que as respostas imunes inatas não podem se adaptar após uma infecção e, após a reinfecção, uma resposta idêntica é desencadeada a cada vez, essa suposição nunca foi seguida em plantas ou imunidade de invertebrados. Além dos estudos sobre as defesas de plantas e hospedeiros invertebrados descritos acima (veja Memória imunológica como uma característica evolutiva adaptativa), vários mecanismos foram propostos para explicar a indução da memória imune inata em invertebrados, incluindo regulação positiva ou "treinamento" de vias regulatórias como como Toll ou Imd (Boutros et al., 2002) e alterações quantitativas e fenotípicas em populações de células imunes (Ro-drigues et al., 2010). Alguns pesquisadores também propuseram a presença de mecanismos geradores de diversidade em insetos. Esses mecanismos candidatos podem envolver proteínas relacionadas ao fibrinogênio com altas taxas de diversificação no nível genômico (Zhang et al., 2004) ou regulação positiva da expressão de receptores específicos, como moléculas de reconhecimento de peptidoglicano e lectinas (Steiner, 2004).
Pistas importantes de que a imunidade inata de vertebrados também possui características adaptativas foram relatadas em estudos experimentais em camundongos. Vários desses estudos mostraram que camundongos de iniciação ou treinamento com ligantes microbianos podem proteger contra infecções letais. Por exemplo, a imunidade treinada induzida por -glucano (derivado de fungos) induz proteção contra infecção bacteriana por Staphylococcus aureus (Di Luzio e Williams, 1978; Marakalala et al, 2013). Da mesma forma, o dipeptídeo muramil do componente peptidoglicano bacteriano induz proteção contra Toxoplasma (Krahenbuhl et al, 1981), e a administração de oligodesoxinucleotídeo CpG protege contra sepse e meningite por Escherichia coli (Ribes et al, 2014). Além disso, a flagelina de bactérias Gram-negativas pode induzir proteção contra a bactéria Gram-positiva Streptococcus pneumoniae (Munoz et al.,2010) e rotavírus (Zhang et al.,2014a). Além dos ligantes microbianos, há evidências de que certas citocinas pró-inflamatórias podem induzir imunidade treinada: a infecção de camundongos com uma dose de IL recombinante-1 três dias antes da infecção com Pseudo-monas aeruginosa protegeu camundongos contra a mortalidade(van der Meer et ai., 1988). O caráter não específico dos efeitos da imunidade treinada argumenta contra um efeito de memória clássico mediado pela imunidade adaptativa e sugere a ativação de mecanismos imunes inatos não específicos. Um aspecto importante que precisará ser investigado é a duração dos efeitos protetores da imunidade treinada. Estudos em camundongos e humanos mostraram efeitos após 3 meses e até um ano (Kleinnijenhuis et al, 2014), embora dados epidemiológicos baseados nos efeitos heterólogos protetores das vacinas sugiram que elas serão funcionais por pelo menos 3-a 5 anos.
A imunidade treinada pode mediar pelo menos alguns dos efeitos protetores da vacinação. Evidências convincentes vêm de estudos que mostram que a vacinação com o bacilo da vacina contra tuberculose Calmette Guerin (BCG), a vacina mais comumente usada em todo o mundo, induz proteção independente de células T contra infecções secundárias por Candida albicans, Schistosoma mansoni ou influenza em animais (Spencer et al. ., 1977; Tribouley et al. 1978; can't Wout et al., 1992). Dados humanos completam esses estudos: a vacinação com BCG em voluntários humanos protege contra uma infecção experimental com o vírus da vacina da febre amarela (Arts et al, 2018), enquanto grandes estudos epidemiológicos relataram efeitos heterólogos protetores para BCG e vacinação contra sarampo (Benn et al, 2013 ; Goodridge et al, 2016). Além disso, a latência do herpesvírus aumenta a resistência aos patógenos bacterianos Listeria monocytogenes e Yersinia pestis (Barton et al., 2007) com proteção alcançada por meio do aumento da produção de IFNy e ativação sistêmica de macrófagos. Da mesma forma, a infecção com o parasita helmíntico Nip-strongyles brasiliensis induz um fenótipo de macrófago de longo prazo que danifica o parasita e induz proteção contra reinfecção independentemente dos linfócitos T e B (Chen et al., 2014).
As principais populações de células que foram relatadas como responsáveis pela memória imune inata são monócitos, macrófagos derivados de monócitos e células natural killer (NK). Enquanto a proteção secundária dependente de macrófagos da infecção é inespecífica, a memória imune mediada por células NK pode fornecer maior especificidade. A primeira evidência de memória de células NK vem de observações de diferentes camundongos com deficiência de células T e B (nocaute RAG, SCID e nu/nu) sendo capazes de montar respostas de recordação robustas a sensibilizadores de contato baseados em hapteno (O'Leary et al, 2006). As células NK podem mediar o contato específico de haptenohipersensibilidade(CHS) nesses animais, mas a memória das células NK é restrita a células residentes no fígado do fenótipo NK.1.1 mais DX5-CXCR6 mais CD49a mais (OLeary et al,2006; Paust et al,2010; Peng et al., 2013). As células NK residentes no fígado de camundongo podem desenvolver memória específica para uma variedade de haptenos e outros antígenos, incluindo partículas semelhantes a vírus (VLPs); no entanto, o mecanismo de reconhecimento do antígeno não é conhecido (Paust et al., 2010). Respostas de células de memória NK específicas de antígeno e de longa duração (esplênicas e hepáticas) também foram observadas em macacos rhesus, sugerindo que células NK de memória específicas de antígeno também podem existir em humanos (Reeves et al., 2015)
As células NK podem ser ativadas por citomegalovírus: após infecção com citomegalovírus murino (mCMV)(Nabekura et al,2015; Schlums et al.,2015; Sun et al,2009; Sunset al.,2012), as células NK portadoras do receptor Ly49H proliferam , persistindo em órgãos linfoides e não linfoides durante a fase de contração da resposta das células NK. Após a reinfecção, as células NK "de memória" sofrem uma expansão secundária, desgranulando rapidamente e liberando citocinas, induzindo assim uma resposta imune protetora (Sun et al, 2009). Vários mecanismos possíveis foram apresentados para explicar as propriedades de memória das células NK, envolvendo o eixo IL-12/IFNy (Sun et al,2012) ou a ativação da molécula coestimuladora DNAM{{10 }} (molécula acessória de DNAx-1, CD226) (Nabekura et al., 2014).

A memória NK induzida por CMV parece ser específica: estudos com camundongos não demonstraram maior capacidade de resposta das células de memória NK induzidas por mCMV contra outras infecções, como influenza ou Listeria (Min-Oo e Lanier, 2014). Da mesma forma, estudos em humanos não mostram nenhuma capacidade de resposta de NKG2C mais CD57 mais população de células NK expandida em humanos (H) CMV mais indivíduos (Hendricks et al, 2014). Células NK preparadas com citocinas também foram sugeridas para desenvolver propriedades semelhantes à memória. Células NK de camundongo e humanas estimuladas com uma combinação de IL12, IL15 e IL18 mostraram maior produção de IFNy em resposta à estimulação secundária com citocinas ou células tumorais semanas após o priming de citocinas (Cooper et al., 2009; Keppel et al, 2013 ; Romee et al., 2012).
As células linfoides inatas do grupo 2 (ILC2) que compartilham o progenitor linfoide comum com as células NK, B e T, não possuem receptores de antígenos, mas podem ser ativadas por citocinas. Eles também mostram o potencial de "lembrar" seu status de ativação e gerar respostas aprimoradas após estimulação secundária. No pulmão, os alérgenos inalados estimulam ILC2s a produzir IL-5 e IL-13 de maneira IL-33-dependente (Halim et al., 2014). Após a ativação induzida por alérgenos, as ILC2s pulmonares sofrem expansão seguida de uma fase de contração na qual não produzem citocinas. Uma população de ILC2s com experiência de alérgenos persiste no pulmão e nos linfonodos. Após um desafio secundário com alérgenos não relacionados, os ILC2s semelhantes à memória montam uma resposta imune mais robusta. A sensibilização de camundongos com IL-33 foi suficiente para gerar ILC2s de memória responsivos à estimulação secundária de alérgenos, indicando o caráter não específico do antígeno da memória de ILC2s (Martinez-Gonzalez et al., 2016).
Essas observações também podem destacar o posicionamento único de ILCs e células NK na encruzilhada evolutiva entre a imunidade inata e adaptativa.
Em conjunto, esses estudos complementares em murinos e humanos demonstram que as respostas imunes inatas têm a capacidade de ser "treinadas" e, assim, exercer um novo tipo de memória imunológica após a reinfecção, para a qual o termo imunidade treinada foi proposto (Netea et al, 2016; Netea et al., 2011). Uma extensão do conceito de imunidade treinada foi recentemente proposta para conter também tipos de células não imunes, como células epiteliais (Cassone, 2018).
