Transição Ativa da Fase de Memória do Medo da Reconsolidação à Extinção através da Prevenção da Reconsolidação Mediada por ERK
Mar 19, 2022
Contato: Audrey Hu Whatsapp/hp: 0086 13880143964 E-mail:audrey.hu@wecistanche.com
A recuperação detemermemóriainduz dois processos de memória opostos, ou seja, reconsolidação e extinção. A recuperação breve induz a reconsolidação para manter ou aumentar o medomemória, enquanto a recuperação prolongada extingue essa memória. Embora os mecanismos de reconsolidação e extinção tenham sido investigados, ainda não se sabe como as fases da memória do medo são alteradas da reconsolidação para a extinção durante a recuperação da memória. Aqui, mostramos que um processo de transição de memória dependente de quinase regulada por sinal extracelular (ERK) após a recuperação regula a mudança de fases de memória de reconsolidação para extinção, impedindo a indução de reconsolidação em uma tarefa de esquiva inibitória (IA) em camundongos machos. Primeiramente, a fase de memória de transição, que cancela a indução da reconsolidação, mas é insuficiente para a aquisição da extinção, foi identificada após a reconsolidação, mas antes das fases de extinção. Em segundo lugar, as fases de reconsolidação, transição e extinção apósrecuperação de memóriamostraram assinaturas moleculares e celulares distintas através da proteína de ligação ao elemento responsiva a cAMP (CREB) e fosforilação ERK na amígdala, hipocampo e córtex pré-frontal medial (mPFC). A fase de reconsolidação mostrou aumento da fosforilação de CREB, enquanto a fase de extinção apresentou várias populações neurais com várias combinações de fosforilação de CREB e/ou ERK, nessas regiões do cérebro. Curiosamente, as três fases de memória, incluindo a fase de transição, mostraram ativação transitória de ERK imediatamente após a recuperação. Mais importante ainda, o bloqueio de ERK na amígdala, hipocampo ou mPFC na fase de memória de transição desinibiu o aprimoramento induzido pela reconsolidação da memória IA. Essas observações sugerem que a via de sinalização ERK regula ativamente a transição da fase de memória da reconsolidação para a extinção e esse processo funciona como um interruptor que cancela a reconsolidação do medomemória.
Palavras-chave: ERK; extinção; memória do medo; reconsolidação; transição
1Departamento de Biociência, Faculdade de Ciências da Vida, Universidade de Agricultura de Tóquio, Tóquio 156-8502, Japão e
2Graduate School of Agriculture and Life Sciences, The University of Tokyo, Tokyo 113-8657, Japão
Declaração de significância
Recuperação da memória do medoinduz dois processos de memória opostos; reconsolidação e extinção. A reconsolidação mantém/melhoramemória do medo, enquanto a extinção enfraquece a memória do medo. Permanece desconhecido como as fases de memória são alteradas de reconsolidação para extinção durante a recuperação. Aqui, identificamos um processo de transição de memória ativa funcionando como um interruptor que inibe a reconsolidação. Esta fase de transição de memória mostrou um aumento transitório da fosforilação da quinase regulada por sinal extracelular (ERK) na amígdala, hipocampo e córtex pré-frontal medial (mPFC). Curiosamente, a inibição de ERK nessas regiões na fase de transição desinibiu o aprimoramento mediado por reconsolidação da memória de evitação inibitória (IA). Esses achados sugerem que o processo de memória de transição regula ativamente a troca de fases de memória de medo da memória de medo, impedindo a indução de reconsolidação através da ativação da via de sinalização ERK.
Introdução
MemóriaA recuperação não é um processo passivo, mas sim um processo dinâmico que permite a manutenção, fortalecimento, enfraquecimento ou alteração/atualização de uma memória original (Misanin et al., 1968; Schneider e Sherman, 1968; Lewis, 1979; Mactutus et al. ., 1979; Gordon, 1981; Nader et al., 2000; Nader e Hardt, 2009; Dudai, 2012; Fukushima et al., 2014). É importante ressaltar que uma memória de medo condicionada recuperada por breve reexposição ao estímulo condicionado (CS) torna-se lábil e requer reconsolidação dependente da expressão gênica para sua manutenção ou aprimoramento (Nader et al., 2000; Dudai, 2002; Kida et al., 2002; Suzuki et al., 2004; Tronel et al., 2005; Fukushima et al., 2014). Por outro lado, a reexposição contínua ou repetida ao SC induz a extinção da memória, o que enfraquece a memória do medo (Pavlov, 1927; Rescorla, 2001; Myers e Davis, 2002). Assim, a recuperação da memória do medo induz dois processos de memória opostos, ou seja, reconsolidação e extinção, embora ambos os processos sejam induzidos pela reexposição a um EC idêntico, mas diferem de acordo com a duração da reexposição ao EC.
A característica bioquímica comum e crítica de reconsolidação e extinção é o requisito para a expressão gênica mediada pela proteína de ligação ao elemento responsiva a cAMP (CREB) (Mamiya et al., 2009). Curiosamente, mostramos assinaturas moleculares, anatômicas e comportamentais contrastantes entre as fases de reconsolidação e extinção da memória contextual do medo (Suzuki et al., 2004; Mamiya et al., 2009). O bloqueio da síntese de proteínas durante a fase de reconsolidação interrompe o medo originalmemória, enquanto o bloqueio da síntese de proteínas durante a fase de extinção não faz isso, embora a memória contextual do medo tenha sido reativada. A exigência de regiões do cérebro exibindo a ativação da expressão gênica mediada por CREB difere entre reconsolidação e extinção; a reconsolidação depende da amígdala e do hipocampo, enquanto a extinção depende da amígdala e do córtex pré-frontal medial (mPFC). No entanto, o curso de tempo de ativação do CREB amigdaloide difere entre as fases de reconsolidação e memória de extinção. Essas observações sugeriram que as fases de reconsolidação e extinção não são independentes, mas interagem entre si. Curiosamente, estudos recentes identificaram uma janela de tempo (fase de transição) que não mostra ativação de quinase regulada por sinal extracelular (ERK) na amígdala após a reconsolidação, mas antes das fases de extinção após a recuperação da memória auditiva do medo (Merlo et al., 2018). ). Tomados em conjunto, esses achados sugerem os possíveis mecanismos pelos quais as fases da memória são alteradas de reconsolidação para extinção durante a recuperação da memória do medo. Em outras palavras, é possível que o processo de transição de memória regule ativamente essa chave.
Em uma tarefa de esquiva inibitória (IA), os camundongos recebem um choque elétrico nas patas depois de entrarem em um compartimento escuro de um compartimento claro e formarmemóriapara evitar o compartimento escuro. Anteriormente, usando esta tarefa, mostramos que as fases de reconsolidação e extinção podem ser discriminadas no momento em que um camundongo entra em um compartimento escuro de um compartimento claro durante uma sessão de reexposição (Fukushima et al., 2014). Portanto, esta tarefa nos permite caracterizar as assinaturas moleculares em perspectiva das fases de reconsolidação e extinção, em contraste com o paradigma clássico de condicionamento contextual do medo em que a reativação da memória do medo condicionado pela reexposição ao CS inicia tanto a reconsolidação quanto a extinção; a reexposição curta (3 min) ao contexto condicionado induz a reconsolidação, enquanto a reexposição longa (30 min) ou repetida a este contexto induz a extinção (Eisenberg et al., 2003; Pedreira e Maldonado, 2003; Suzuki et al., 2004; Lee et al., 2008; Mamiya et al., 2009). Além disso, descobrimos que a memória IA recuperada é aprimorada por meio da reconsolidação da memória nesta tarefa (Fukushima et al., 2014).
Compreender o mecanismo de transição da reconsolidação para a extinção durante a recuperação do medomemória, nosso objetivo foi identificar e caracterizar as assinaturas moleculares, celulares e comportamentais das fases de reconsolidação, transição e extinção da memória IA. Analisamos a ativação de CREB e ERK na amígdala, hipocampo e mPFC nas fases de reconsolidação, transição e extinção e examinamos os papéis da ativação de ERK nesses processos de memória.

Materiais e métodos
Ratos Todos os experimentos foram conduzidos de acordo com o Guia para o Cuidado e Uso de Animais de Laboratório (Japan Neuroscience Society e Tokyo University of Agriculture). Todos os experimentos com animais realizados neste estudo foram aprovados pelo Comitê de Cuidados e Uso de Animais da Universidade de Agricultura de Tóquio (autorização nº 280037). Todos os procedimentos cirúrgicos foram realizados sob anestesia com Nembutal e todos os esforços foram feitos para minimizar o sofrimento. Camundongos machos C57BL/6N foram obtidos de Charles River. Os camundongos foram alojados em gaiolas de cinco ou seis, mantidos em um ciclo claro/escuro de 12/12 h, com acesso a comida e água ad libitum. Os camundongos tinham pelo menos oito semanas de idade quando testados. O teste foi realizado durante a fase leve do ciclo. Todos os experimentos foram conduzidos cegos para a condição de tratamento dos camundongos.
Teste IA O aparelho IA de passagem (OHARA Pharmaceutical) consistia em uma caixa com compartimentos claros e escuros separados (ambos 15,5 12,5 11,5 cm). O compartimento de luz foi iluminado por uma luz fluorescente (2500 lux; Fukushima et al., 2008, 2014; Zhang et al., 2011; Ishikawa et al., 2016). Antes do início do treinamento IA, os camundongos foram manuseados individualmente por 2 minutos a cada dia durante uma semana. Durante as sessões de treinamento, cada camundongo foi habituado ao compartimento claro por 30 s, e a porta da guilhotina foi levantada para permitir o acesso ao compartimento escuro. A latência para entrar no compartimento escuro foi considerada como uma medida de aquisição. Assim que o rato entrou no compartimento escuro, a porta da guilhotina foi fechada. Após 5 s, um choque no pé (0,2 mA) foi aplicado por um período total de 2 s (treinamento). Às 24 h após a sessão de treinamento, o mouse foi colocado de volta no compartimento claro até entrar no compartimento escuro (média 459 6 15,49 s). Imediatamente após o camundongo ter entrado no compartimento escuro, a porta da guilhotina foi fechada e o camundongo permaneceu no compartimento escuro por um período de tempo variável (0, 1 ou 10 min) sem choque nas patas (reativação). A memória foi avaliada 48 h depois [teste de memória de longo prazo pós-reativação (PR-LTM)] como a latência de cruzamento para o camundongo entrar no compartimento escuro quando recolocado no compartimento claro, como na reativação.
Para o primeiro experimento, examinamos o efeito da inibição da síntese proteica após a reativação (reexposição ao compartimento escuro por 0, 1 ou 10 min; Fig. 1). O inibidor da síntese proteica anisomicina (ANI; Wako) foi dissolvido em solução salina (pH ajustado para 7.0–7,4 com NaOH). Os camundongos foram treinados conforme descrito acima e, 24 h depois, receberam veículo (VEH) ou ANI (150 mg/kg, ip) imediatamente após a reexposição ao compartimento escuro por 0, 1 ou 10 min sem choque nas patas (reativação). Nesta dose, o ANI inibe 0,90 por cento da síntese de proteínas no cérebro durante as primeiras 2 h (Flood et al., 1973). Às 48 h após a sessão de reativação, os camundongos individuais foram novamente colocados no compartimento de luz e a latência de cruzamento foi avaliada.
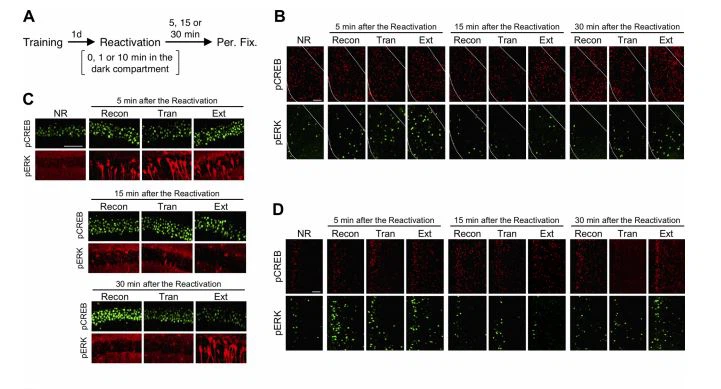
Para o segundo experimento [imuno-histoquímica de CREB fosforilado (pCREB) e ERK fosforilado (pERK); Figs. 2-5], examinamos as regiões do cérebro que foram ativadas após a reexposição à luz (até os camundongos entrarem no compartimento escuro, reexposição ao compartimento escuro por 0 min) ou compartimento escuro (re- exposição ao compartimento escuro por 1 ou 10 min). Os camundongos foram divididos em quatro Fukushima et al. · Transição das fases da memória do medo após a recuperação J. Neurosci., 10 de fevereiro de 2021, • 41(6):1288–1300 • 1289grupos. Às 24 h após o treinamento, os camundongos individuais foram reexpostos ao compartimento claro e, em seguida, permaneceram no compartimento escuro após sua entrada no compartimento escuro [reativação: 0 min no compartimento escuro, grupo reconsolidação (Recon); 1 min, grupo de transição (Tran); 10 min, grupo de extinção (Ext)]. Outro grupo de camundongos não retornou ao compartimento claro/escuro [grupo não reativado (NR)]. Os camundongos foram então anestesiados com Nembutal (750 mg/kg, ip) em 5, 15 ou 30 min após a reativação.
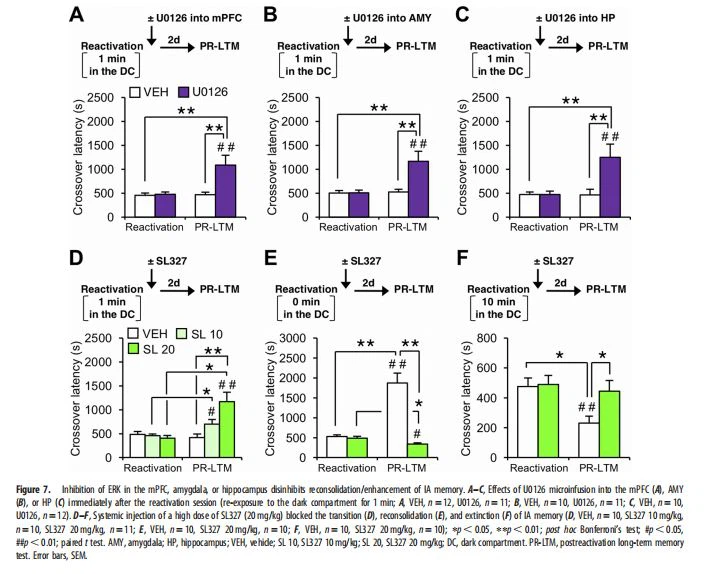
Para o terceiro experimento (microinfusão de U0126; Figs. 6,7), examinamos os efeitos da inibição de ERK na amígdala, hipocampo ou mPFC emmemóriareconsolidação/aprimoramento, transição e extinção. O inibidor de MEK U0126 (Sigma-Aldrich) foi dissolvido em líquido cefalorraquidiano artificial contendo três gotas de Tween 80 (Sigma) em 2,5 ml de 7,5 por cento de dimetilsulfóxido (Wako) e ajustado para pH 7,4 com NaOH. Os camundongos foram treinados conforme descrito acima e, 24 horas depois, foram colocados de volta no compartimento de luz (reativação). Os camundongos foram microinfundidos com U0126 (1 mg) ou VEH nas várias regiões do cérebro imediatamente após (Figs. 6A, C, E–H, 7A–C) ou em 30 min após (Fig. 6B, D) reativação. Às 48 h após a reativação, os camundongos individuais foram novamente colocados no compartimento de luz e a latência de cruzamento foi avaliada (PR LTM). Microinfusões no hipocampo e mPFC (0,5 ml) foram feitas a uma taxa de 0,25 ml/min. Microinfusões na amígdala (0,2 ml) foram feitas a uma taxa de 0,1 ml/min. A cânula de injeção foi deixada no local por 2 minutos após a microinfusão e os camundongos foram então devolvidos às suas gaiolas. O inibidor de MEK SL327 (Santa Cruz Biotechnology) foi dissolvido em dimetilsulfóxido e diluído com solução salina. Os camundongos foram treinados como descrito acima e, 24 h depois, os camundongos individuais foram colocados de volta no compartimento de luz (reativação). Os camundongos foram injetados sistemicamente com SL327 (10 ou 20 mg/kg) ou VEH imediatamente após a reativação (Fig. 7D-F). Às 48 h após a reativação, os camundongos individuais foram novamente colocados no compartimento de luz e a latência de cruzamento foi avaliada (PR-LTM).
A imunohistoquímica foi realizada conforme descrito anteriormente (Mamiya et al., 2009; Suzuki et al., 2011; Zhang et al., 2011; Fukushima et al., 2014; Ishikawa et al., 2016; Hasegawa et al., 2019). Após anestesia, todos os camundongos foram perfundidos com 4% de paraformaldeído. Os cérebros foram removidos, fixados durante a noite, transferidos para 30% de sacarose e armazenados a 4 graus. Cortes coronais (30 mm) foram cortados em um criostato.
Para coloração de pCREB e pERK, as seções de flutuação livre foram tratadas com 1 por cento de H2O2 e incubadas durante a noite com um anticorpo policlonal de coelho anti-fosfo-CREB (serina 133; S133) (1:1000; #{{10) }}, Millipore) e/ou anticorpo monoclonal de coelho anti-fosfo-ERK1/2 (T202/Y204) (1:300; #4370; Tecnologia de Sinalização Celular) em solução de bloqueio (solução salina tamponada com fosfato mais 1 por cento de albumina de soro de cabra, 1 mg/ml de albumina de soro bovino e 0,05 por cento de Triton X-100). As seções foram lavadas com solução salina tamponada com fosfato e incubadas com IgG anti-coelho de burro conjugado com peroxidase de rábano (1:500; Jackson ImmunoResearch) para pCREB ou IgG anti-coelho de cabra conjugado com peroxidase de rábano para pERK por 1 h em temperatura ambiente. Os sinais de pCREB foram amplificados por biotina tiramida e visualizados usando estreptavidina conjugada com Alexa Fluor (Invitrogen). Os sinais de pERK foram amplificados com TSA-FCM (Invitrogen). Os cortes foram montados em lâminas e lamínulas utilizando um meio de montagem (Millipore).
A quantificação foi realizada conforme descrito anteriormente (Frankland et al., 2006; Fukushima et al., 2014; Mamiya et al., 2009; Zhang et al., 2011; Suzuki et al., 2008). As estruturas foram definidas anatomicamente de acordo com o atlas de Franklin e Paxinos (1997). Todos os neurônios imunorreativos foram contados por um experimentador cego para a condição de tratamento

Resultados
Caracterização das fases da memória após a recuperação na tarefa IA
A tarefa de IA nos permite discriminar as fases de reconsolidação e extinção no momento em que um camundongo entra em um compartimento escuro de um compartimento claro (Fukushima et al., 2014). Para entender o mecanismo subjacente à mudança das fases de memória de reconsolidação para extinção, caracterizamos as fases de memória IA após a recuperação da memória examinando os efeitos da inibição da síntese proteica que é necessária para a reconsolidação e extinção da memória IA (Fukushima et al., 2014). Os camundongos foram colocados primeiro no compartimento de luz. Aos 5 s após entrarem no compartimento escuro, foi aplicado um breve choque elétrico nas patas (treinamento). Os camundongos foram reexpostos ao compartimento claro 24 h após o treinamento (sessão de reativação; Fig. 1A) e sua latência de cruzamento para entrar no compartimento escuro foi avaliada (Fig. 1B). Os camundongos foram devolvidos às suas gaiolas imediatamente após entrarem no compartimento escuro do compartimento claro (0-min reexposição ao compartimento escuro; fase de reconsolidação) ou permaneceram no compartimento escuro por 1, 3 ou 10 min sem receber um choque nos pés (fase de extinção; Fig. 1C–E). Imediatamente após a sessão de reativação, os camundongos receberam uma injeção sistêmica de VEH ou do inibidor de síntese proteica ANI. Após 48 h, a latência do cruzamento foi avaliada PR-LTM.
Consistente com nosso estudo anterior (Fukushima et al., 2014), a reexposição ao compartimento de luz (grupo 0 min) induziu a reconsolidação e o aprimoramento da memória IA. Uma ANOVA bidirecional revelou efeitos significativos de tempo (F(1,24)=10.433, p=0.{{20}}036), droga (F(1 ,24)=23.197, p, 0,0001) e tempo de interação medicamentosa (F(1,24)=25.022, p, 0,0001; Fig. 1B). O teste post hoc de Bonferroni e o teste t pareado revelaram que os grupos VEH e ANI apresentaram latência de cruzamento significativamente aumentada ou diminuída, respectivamente, no PR-LTM em comparação com a sessão de reativação (ps , 0,05; VEH, t(6) {{28 }} 5,134, p=0.0021, ANI, t(6)=4.804, p=0.003; Fig. 1B). Essas observações indicam que a recuperação da memória IA no compartimento de luz melhorou a memória, enquanto a inibição da síntese proteica interrompeu a memória recuperada, confirmando a observação anterior de que a recuperação da memória IA aumenta a memória através da reconsolidação de uma maneira dependente da síntese proteica.
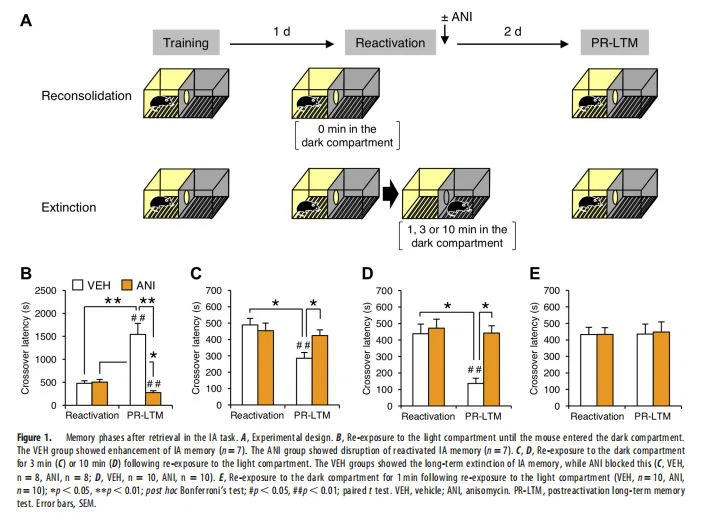
Em contraste, a reexposição ao compartimento escuro induziu extinção a longo prazo [ANOVA de duas vias, tempo (Fig. 1C, F(1,28)=9.575, p=0.{ {50}}04; Fig. 1D, F(1,36)=11.699, p=0.0016), droga (Fig. 1C, F(1,28)=4.674, p=0.039; Fig. 1D, F(1,36)=12.285, p {{29 }}.0012), tempo de interação medicamentosa (Fig. 1C, F(1,28)=7.916, p=0.009; Fig. 1D, F(1,36) {{41 }}.915, p=0.0079)], conforme observado anteriormente (Fukushima et al., 2014). Os grupos VEH que permaneceram no compartimento escuro por 3 ou 10 minutos apresentaram latência de cruzamento significativamente diminuída no PR-LTM em comparação com a sessão de reativação, enquanto os grupos ANI apresentaram latência de cruzamento comparável no PR-LTM em comparação com a sessão de reativação e com a sessão de reativação. Grupos VEH (teste post hoc de Bonferroni, ps, 0,05; teste t pareado, Fig. 1C, VEH, t(7)=4.976, p=0.0016, ANI, t(7) { {59}} 0,796, p. 0,05; Fig. 1D, VEH, t(9)=10,211, p, 0,0001, ANI, t(9)=1,02, p. 0,05 ). Essas observações indicam que a reexposição ao compartimento escuro por 3 ou 10 minutos extinguiu a memória IA e que a inibição da síntese proteica bloqueou a extinção a longo prazo. Assim, a recuperação da memória IA no compartimento escuro extingue a memória IA de uma maneira dependente da expressão gênica.
É importante ressaltar que o grupo VEH mostrou latência cruzada comparável no PR-LTM em comparação com a sessão de reativação e com o grupo ANI quando permaneceram no compartimento escuro por 1 min [ANOVA de duas vias, tempo (F(1,36) {{ 5}}.03, p . 0.05), droga (F(1,36)=0.019, p . 0.05), tempo de interação medicamentosa (F(1,36)=0.011, p. 0,05); teste post hoc de Bonferroni, ps . 0,05; teste t pareado, VEH, t(9)=0.091, p . 0,05, ANI, t(9)=0,328, p. 0,05; Fig. 1E]. Essas observações indicam que o grupo VEH não apresentou aumento nem extinção da memória IA e que o grupo ANI não apresentou interrupção da memória IA. Portanto, a reexposição ao compartimento escuro por 1 min bloqueou tanto o aprimoramento quanto a interrupção induzida por ANI da memória IA reativada, mas não extinguiu a memória IA, sugerindo que essa 1-reexposição min cancela a indução da reconsolidação , mas é insuficiente para extinguir a memória IA.
Em resumo, esses resultados indicaram que a reexposição ao compartimento claro induz a fase de reconsolidação, enquanto a reexposição mais longa ao compartimento escuro (3 ou 10 min) induz a fase de extinção. Mais importante, permanecer por 1 min no compartimento escuro induz a fase de transição da reconsolidação para a extinção, que inibe a reconsolidação da memória de medo sem induzir a extinção.
Assinaturas moleculares das fases de reconsolidação, transição e extinção na amígdala, hipocampo e mPFC após recuperação de memória IA
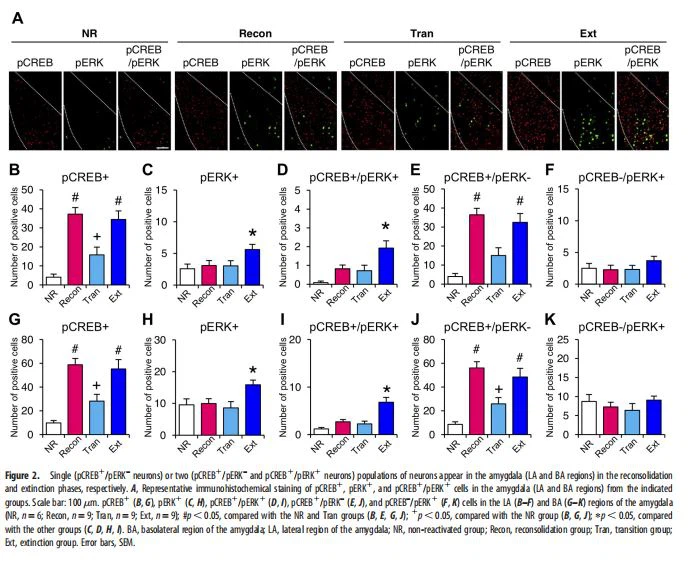
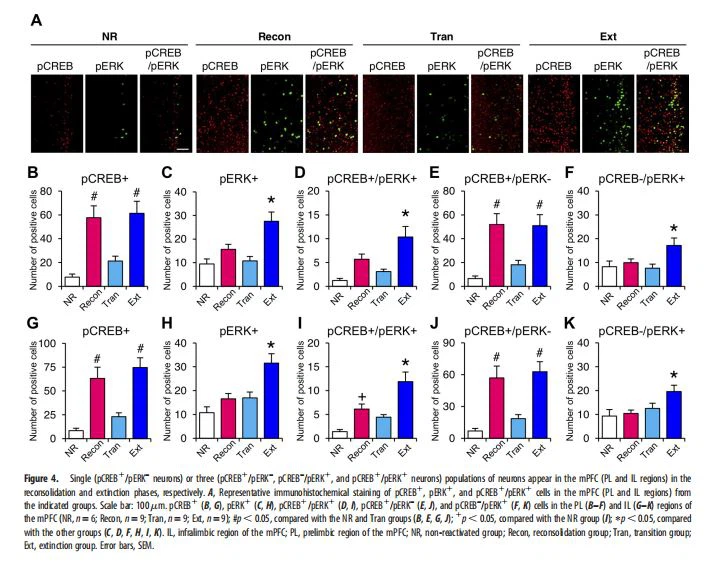
A reconsolidação e a extinção da memória contextual de medo mostram aumentos na fosforilação de CREB em S133, um marcador de ativação da expressão gênica necessária para reconsolidação e extinção de longo prazo, mas mostram dinâmicas distintas de fosforilação de CREB (Mamiya et al., 2009 ). Curiosamente, estudos recentes mostraram que não há aumento na fosforilação de ERK, um regulador a montante de CREB (Impey et al., 1998; Wu et al., 2001), na região basolateral da amígdala na transição da reconsolidação à extinção de uma memória de medo sinalizada, embora essa fosforilação seja aumentada na região basolateral quando uma memória de medo sinalizada é reconsolidada e extinta (Merlo et al., 2014, 2018). Outro estudo indicou que o ERK hipocampal é ativado apenas quando a memória contextual do medo é extinta, mas não reconsolidada (Tronson et al., 2009). Esses achados sugerem que as fases de reconsolidação, transição e extinção apresentam assinaturas moleculares e celulares distintas. Portanto, medimos e comparamos os níveis de pCREB e pERK nas fases de reconsolidação, transição e extinção usando imuno-histoquímica. Realizamos esquemas experimentais semelhantes aos da Figura 1B, D, E usando quatro grupos experimentais. Os camundongos foram reexpostos ao compartimento claro 24 h após o treinamento e então permaneceram no compartimento escuro [reativação: 0 min no compartimento escuro, grupo reconsolidação (Recon); 1 min, grupo de transição (Tran); 10 min, grupo de extinção (Ext)]. Outro grupo de camundongos não retornou ao compartimento claro/escuro (não reativado, grupo NR). Contamos neurônios pCREB-positivos (pCREB1), neurônios pERK-positivos (pERK1) e neurônios duplo-positivos (pCREB1/pERK1) na amígdala, hipocampo e mPFC 30 minutos após a sessão de reativação.
Amígdala (região lateral) CREB foi ativado nas fases de extinção e reconsolidação, enquanto ERK foi ativado apenas na fase de extinção (Fig. 2A-C). Uma ANOVA unidirecional revelou um efeito significativo de grupo (Fig. 2B, F(3,29)=14.85, p , 0.0001). Semelhante às descobertas anteriores (Mamiya et al., 2009), o teste post hoc Newman-Keuls revelou que os grupos Recon e Ext mostraram significativamente mais neurônios pCREB1 do que os outros grupos (p, 0,05). Essas observações indicaram que, semelhante às observações nos níveis comportamentais (Fig. 1), a exposição ao compartimento escuro por 1 min (fase de transição) cancela a "ligação" da fosforilação de CREB que seria aumentada na fase de reconsolidação. Em contraste, significativamente mais neurônios pERK1 foram observados no grupo Ext do que nos outros grupos, embora houvesse muito menos neurônios pERK1 do que neurônios pCREB1 no grupo Ext (F(3,29)=3.793, p { {23}}.0207; Fig. 2C).
Consistentemente, significativamente mais neurônios positivos duplos (pCREB1/pERK1) foram observados no grupo Ext (F(3,29)=6.698, p=0.00 14; Fig. 2D), enquanto significativamente mais neurônios pCREB1/pERK– (pCREB único positivo) foram observados nos grupos Recon e Ext (F(3,29)=13.689, p , 0 .0001; Fig. 2E). Assim, a fase de reconsolidação mostrou apenas uma única população de neurônios pCREB1/pERK–. Em contraste, a fase de extinção mostrou duas populações de neurônios pCREB1/pERK– e pCREB1/pERK1, indicando que ERK é ativado apenas em um subconjunto de neurônios pCREB1. Importante, resultados semelhantes foram observados na região basolateral da amígdala (Fig. 2G, F(3,29)=13.042, p, 0,0001; Fig. 2H, F(3,29) {{32} },824, p=0,0201; Fig. 2I, F(3,29)=12,633, p, 0,0001; Fig. 2J, F(3,29)=12 0,505, p, 0,0001).
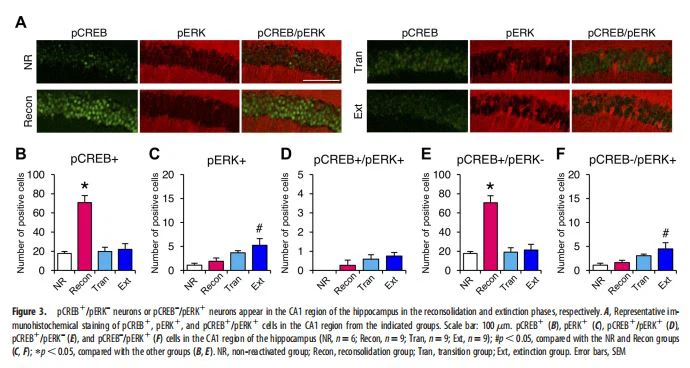
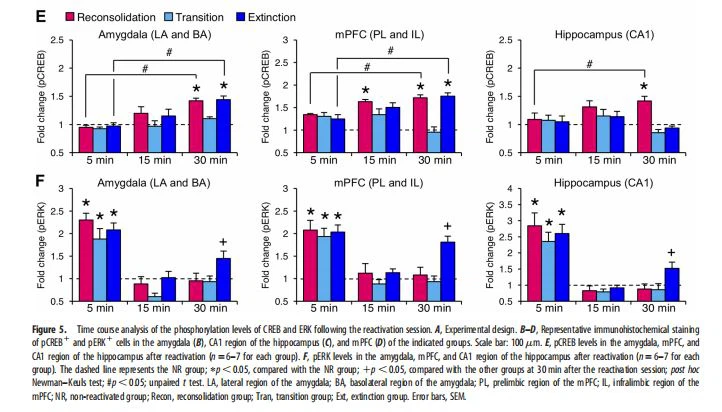
A ativação bifásica de ERK na fase de extinção ERK é um ativador upstream de CREB e, portanto, a ativação de ERK é necessária para a consolidação e reconsolidação da memória do medo (Schafe et al., 200{{31 }}; Duvarci et al., 2005). No entanto, de forma inconsistente, nenhuma ativação de ERK foi observada na amígdala, hipocampo ou mPFC na fase de reconsolidação quando o pERK foi medido em 30 min após a sessão de reativação (Figs. 2-4). Portanto, examinamos os cursos de tempo de fosforilação de ERK e CREB. Realizamos um experimento semelhante ao das Figuras 2-4, exceto que os níveis de pCREB e pERK foram medidos em 5, 15 e 30 min após a sessão de reativação (reexposição ao compartimento escuro por {{ 66}}, 1 ou 10 min; Fig. 5A). Consistente com os dados mostrados nas Figuras 2-4, aumentos significativos nos neurônios pCREB1 foram observados em 30 min, mas não em 5 min, após a sessão de reativação no Recon (amígdala, mPFC e hipocampo) e Ext (amígdala e mPFC ), mas não o grupo Tran (Fig. 5E, ANOVA unidirecional, amígdala, 5 min, F(3,23)=0.346, p. 0,05, 30 min, F(3,23)=15,272, p, 0,0001; mPFC, 5 min, F(3,23)=1.169, p. 0,05, 30 min, F(3,23)=32. 346, p, 0,0001; hipocampo, 5 min, F(3,23)=0,154, p. 0,05, 30 min, F(3,23)=16,197, p, 0,0001; teste t não pareado, amígdala, reconsolidação, 5 vs 30 min, t(12)=7 .807, p , 0.0001, extinção, 5 vs 30 min, t(12)=5 .405, p { {73}} 0,0002; mPFC, reconsolidação, 5 vs 30 min, t(12)=5 0,727, p, 0,0001, extinção, 5 vs 30 min, t(12)=4,188 , p=0.0013; região CA1 do hipocampo, reconsolidação, 5 vs 30 min, t(12)=2.339, p=0.0374).
Curiosamente, aumentos significativos nos neurônios pERK1 foram observados na amígdala, mPFC e hipocampo dos grupos Recon, Tran e Ext 5 min após a sessão de reativação em comparação com o grupo NR (Fig. 5F, amígdala, F(3,23)=10.961, p=0.0001; mPFC, F(3,23)=7.525, p { {13}}.0011; hipocampo, F(3,23)=6.924, p=0.0017). Essas observações indicaram que o ERK é ativado imediatamente após a sessão de reativação em todas as fases da memória. No entanto, esses aumentos no número de neurônios pERK1 retornaram aos níveis basais (comparáveis com o grupo NR) em 15 minutos após a sessão de reativação (Fig. 5F, amígdala, F(3,20)=2.676, p 0,05; mPFC, F(3,23)=0,683, p. 0,05; hipocampo, F(3,20)=0,74, p. 0,05). Além disso, consistente com os achados mostrados nas Figuras 2-4, significativamente mais neurônios pERK1 foram observados na amígdala, mPFC e hipocampo em 30 minutos após a sessão de reativação apenas no grupo Ext (Fig. 5F, amígdala, F( 3,23)=6,616, p=0,022; mPFC, F(3,23)=8,012, p=0,0008; hipocampo, F( 3,23)=6.206, p=0.003). Assim, as fases de reconsolidação e transição mostram ativação transitória de ERK apenas no ponto de tempo inicial (5 min), enquanto a fase de extinção mostra ativação bifásica de ERK nos pontos de tempo inicial (5 min) e tardio (30 min) após a reativação sessão. Essas observações indicaram que os mecanismos de regulação da ativação de ERK diferem nas fases de reconsolidação/transição e extinção. Coletivamente, nossas observações demonstraram que as fases de reconsolidação, transição e extinção apresentam assinaturas moleculares distintas.
Papéis da ativação de ERK nas fases de reconsolidação e extinção da memória IA
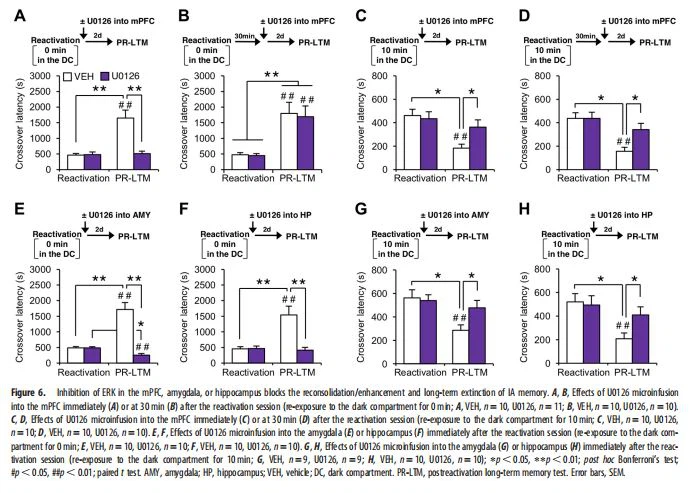
As fases de reconsolidação/transição e extinção apresentaram ativação ERK monofásica e bifásica, respectivamente. Em seguida, investigamos e comparamos os papéis da ativação de ERK precoce (5 min) e tardia (30 min) no mPFC nas fases de reconsolidação e extinção examinando os efeitos da inibição de ERK (Fig. 6).
Discussão
Neste estudo, investigamos os mecanismos de transição da memória da fase de reconsolidação para a de extinção após a recuperação da memória IA. Primeiro caracterizamos as assinaturas comportamentais das fases de memória IA após a recuperação. Consistente com nosso estudo anterior (Fukushima et al., 2014), reconsolidação e extinção induzidas por recuperação de memória IA por reexposição à luz (0 min no compartimento escuro) e escuro ( 3 ou 10 min), respectivamente. Curiosamente, a memória IA não foi aprimorada nem extinta e mostrou resistência à inibição da síntese de proteínas quando os camundongos foram reexpostos ao compartimento escuro por apenas 1 minuto. Portanto, essas observações sugerem que uma reexposição 1-min ao compartimento escuro cancela a indução da reconsolidação, mas é insuficiente para extinguir a memória IA. Além disso, descobrimos que ERK foi ativado na amígdala, hipocampo e mPFC em um ponto de tempo inicial (5 min) após a reexposição ao compartimento escuro por 0, 1 ou 10 min. Consistentemente, a inibição de ERK nessas regiões do cérebro bloqueou a reconsolidação/aprimoramento e extinção da memória IA. Mais importante ainda, a inibição de ERK na amígdala, hipocampo e mPFC após 1-min reexposição ao compartimento escuro desinibiu o aprimoramento mediado por reconsolidação da memória IA, sugerindo que a ativação de ERK após breves (1 min) reexposições para o compartimento escuro é necessária para a inibição da reconsolidação da memória IA. Por outro lado, uma reexposição 1-min ao compartimento escuro foi insuficiente para extinguir a memória IA, embora a reexposição estendida ao compartimento escuro (3 ou 10 min) tenha extinguido essa memória. Portanto, nossos resultados sugerem que uma reexposição 1-min ao compartimento escuro induz um processo de transição de memória que cancela a reconsolidação/aprimoramento, mas não inicia o aprendizado de extinção. Coletivamente, sugerimos que o processo de transição da memória contribui para a mudança das fases da memória de reconsolidação para extinção através da prevenção de reconsolidação mediada por ERK.
Semelhante às nossas observações atuais, um estudo recente usando condicionamento auditivo de medo mostrou que apresentações únicas (1) ou prolongadas (10) de CS induzem a reconsolidação e extinção da memória, respectivamente, por meio de um aumento dos níveis de pERK na região basolateral da amígdala. Em contraste, apresentações intermediárias (4-7) CS não alteram os níveis de pERK na região basolateral da amígdala. É importante ressaltar que a inibição de ERK nas apresentações intermediárias de CS não afetou a memória do medo. Este estudo sugeriu que há uma transição da fase de memória da reconsolidação para a extinção após a recuperação da memória do medo (Merlo et al., 2018). No presente estudo, estendemos essa descoberta e sugerimos que a fase de transição muda ativamente as fases de memória de reconsolidação para extinção por meio da ativação da via de transdução de sinal ERK. Em contraste com descobertas anteriores (Merlo et al., 2018), descobrimos que a fase de transição envolve a fosforilação de ERK na amígdala, hipocampo e mPFC. Essas discrepâncias podem ser devido à diferença de pontos de tempo examinando a fosforilação de ERK; o estudo anterior mediu os níveis de pERK em 12 min após a apresentação do CS (Merlo et al., 2018), enquanto nosso estudo mostrou que os níveis aumentados de pERK retornaram ao nível basal por volta desse ponto de tempo (15 min após a reexposição). Além disso, é importante notar que a tarefa IA permite a observação do aprimoramento da memória IA através da reconsolidação, levando assim à nossa descoberta de que a inibição de ERK na fase de transição desinibe o aprimoramento da memória IA.
Estudos anteriores mostraram que a fosforilação de ERK é aumentada na região basolateral da amígdala em 20 a 60 minutos após o aprendizado da extinção da memória de medo (Herry et al., 2006; Merlo et al., 2014, 2018), enquanto o hipocampo mostra esta ativação em 1 h após o aprendizado da extinção da memória contextual do medo (Fischer et al., 2007; Tronson et al., 2009). No presente estudo, obtivemos observações semelhantes de que o pERK aumenta 30 minutos após a sessão de reativação na fase de extinção. Esses achados sugerem que a fosforilação ERK é uma assinatura molecular comum da fase de extinção tardia (20-60 min).
Além disso, observamos que a ativação de ERK ocorre bifásicamente nos momentos iniciais e tardios (5 e 30 min) após a sessão de reativação na fase de extinção, enquanto essa ativação ocorre monofásicamente no momento inicial da fase de reconsolidação (Fig. 5) . Consistentemente, a inibição de ERK em regiões do cérebro nesses pontos de tempo das fases de reconsolidação e extinção bloqueou a reconsolidação/aumento e a extinção de longo prazo, respectivamente (Fig. 6A, C-H). Essas observações sugerem que a ativação ERK monofásica e bifásica é necessária para o aprimoramento mediado por reconsolidação e extinção da memória IA, respectivamente. É importante notar que ERK funciona como um regulador a montante da fosforilação de CREB. Portanto, a ativação transitória de ERK na fase inicial de memória pode, pelo menos em parte, contribuir para essa fosforilação de CREB, que ativa a expressão de genes necessários para reconsolidação e extinção em longo prazo.

Semelhante aos nossos achados anteriores usando condicionamento contextual do medo (Mamiya et al., 2009), o CREB foi ativado nas fases de reconsolidação (amígdala/hipocampo/mPFC) e extinção (amígdala/mPFC), enquanto o ERK foi ativado apenas na fase de extinção 30 min após a sessão de reativação. Consistentemente, apenas uma única população de neurônios pCREB1/pERK– foi observada na fase de reconsolidação, enquanto populações distintas de neurônios foram observadas na fase de extinção: neurônios pCREB1/pERK– e pCREB1/pERK1 na amígdala (Fig. 2); neurônios pCREB– /pERK1 no hipocampo (Fig. 3); e neurônios pCREB1/pERK–, pCREB– /pERK1 e pCREB1/pERK1 no mPFC (Fig. 4). Essas observações, especialmente a observação contrastante dos neurônios pCREB–/pERK1 e pCREB1/pERK–, sugerem que a ativação de CREB e ERK é regulada de forma diferente em cada área do cérebro quando a memória é extinta e que a ativação da fase tardia de ERK desempenha um papel específico e distinto. papéis para a extinção da memória do medo em comparação com outros processos de memória, como consolidação e reconsolidação, conforme discutido abaixo. Curiosamente, observamos que os neurônios pERK1 foram mais abundantes no mPFC em comparação com o hipocampo e amígdala, uma vez que o mPFC apresentou uma maior proporção de neurônios pERK1 (fase de extinção) e neurônios pCREB1 (fase de reconsolidação) em comparação com o hipocampo e a amígdala, sugerindo que a ativação de ERK no mPFC desempenha um papel mais específico na extinção da memória.
Ainda não está claro se as mesmas ou diferentes populações de neurônios são ativadas nas fases de reconsolidação, transição e memória de extinção. Um estudo anterior identificou a ativação de "neurônios do medo" e "neurônios de extinção" na amígdala quando a memória do medo é reativada ou extinta, respectivamente (Herry et al., 2008). Portanto, é possível que ERK e CREB sejam ativados nas diferentes populações de neurônios com diferentes perfis temporais (ou seja, "neurônios de reconsolidação" e neurônios de extinção). Como discutido acima, os neurônios pCREB1, incluindo os neurônios pCREB1/pERK1, podem regular a reconsolidação e a extinção a longo prazo da memória IA através da ativação da expressão gênica como neurônios de reconsolidação e extinção, respectivamente. Por outro lado, a ativação de ERK em neurônios pCREB– /pERK1 pode contribuir para o cancelamento da ativação transcricional mediada por CREB que seria necessária para a reconsolidação, uma vez que essa ativação de ERK é observada especificamente na fase de extinção tardia; ERK ativou nos neurônios de reconsolidação para cancelar a ativação da expressão gênica na fase de extinção. Curiosamente, um estudo anterior mostrou que a ativação de ERK hipocampal bloqueia a indução de c-fos quando a memória contextual de medo é extinta (Guedea et al., 2011), levantando a possibilidade de que essa ativação de ERK antagonize a via de sinalização CREB. É importante identificar as populações neuronais que regulam a reconsolidação, transição e extinção e investigar as assinaturas moleculares e o significado funcional desses neurônios. Além disso, as interações entre as populações neurais identificadas neste estudo permanecem desconhecidas. É possível que "neurônios de extinção (transição)" modulam a função dos neurônios de reconsolidação para cancelar impedir a reconsolidação por meio de interações entre eles (Eisenberg et al., 2003; Merlo et al., 2014). Portanto, também é importante examinar essas interações dentro e entre a amígdala, mPFC e hipocampo.
Anteriormente, mostramos que o hipocampo não exibe nenhuma alteração na fosforilação de CREB e expressão de Arc após a extinção do aprendizado do medo contextual e, consistentemente, a inibição da síntese de proteínas no hipocampo na fase de extinção não consegue bloquear a extinção a longo prazo (Mamiya et al. , 2009). Essas observações levantaram a possibilidade de que o hipocampo não seja necessário para a extinção a longo prazo. No entanto, mostramos que ERK é ativado no hipocampo após o aprendizado da extinção da memória IA e, consistentemente, bloquear a ativação de ERK no hipocampo prejudica a extinção a longo prazo. Portanto, nossas observações atuais indicam papéis essenciais para o hipocampo na extinção da memória. Em conjunto com nossas descobertas anteriores, sugerimos que o hipocampo é necessário para a extinção da memória, mas não para um processo semelhante à consolidação para estabilizar uma "memória de extinção" por meio da ativação da expressão gênica.


